Dr Robot - początki medycznej robotyki

W ramach tego projektu przygotowano dwadzieścia robotów Nao, które umieszczono w szpitalu z dziećmi cierpiącymi na cukrzycę. Zaprogramowano im funkcje czysto towarzyskie, wyposażono je w umiejętności rozpoznawania mowy i ekspresji twarzy, a także w rozmaite zadania dydaktyczne związane z informacją o cukrzycy, jej przebiegu, objawach i sposobach leczenia.
Sympatyczne roboty w roli towarzyszy szpitalnej niedoli to uroczy pomysł, ale zewsząd nadchodzą doniesienia o tym, że roboty na serio biorą się już za prawdziwą medyczną robotę. Jest wśród nich np. Veebot, stworzony przez kalifornijski startup. Jego zadaniem jest pobieranie krwi do analizy (3).
Urządzenie wyposażono w system "widzenia" w zakresie podczerwieni i namierzania za pomocą kamery odpowiedniej żyły. Gdy ją już znajdzie, bada ją dodatkowo za pomocą ultradźwięków, sprawdzając, czy nadaje się do zagłębienia igły. Jeśli wszystko się zgadza, wbija igłę i pobiera próbkę krwi.
Cała procedura trwa ok. minuty. Trafność wyboru naczynia krwionośnego u Veebota wynosi 83 procent. Mało? Pielęgniarka dokonująca tego ręcznie ma podobny wynik. A w dodatku zanim Veebot trafi do testów klinicznych, ma przekroczyć 90 procent.
Miały pracować w kosmosie
Pomysł na budowę robotów chirurgicznych oraz tzw. inteligentnych sal operacyjnych powstał w amerykańskiej agencji NASA w latach 80. i 90. XX w. Miały one stanowić wyposażenie statków kosmicznych i baz orbitalnych biorących udział w programach podboju kosmosu.
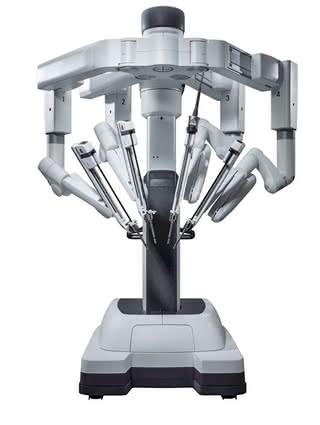
Chociaż programy upadły, naukowcy z Intuitive Surgical nadal pracowali nad robotami chirurgicznymi, a ich działania finansowały prywatne firmy. W efekcie powstał da Vinci, którego po raz pierwszy zaprezentowano pod koniec lat 90. w Kalifornii.
Najpierw jednak, pierwszym na świecie robotem chirurgicznym zatwierdzonym i dopuszczonym do użytku w 1994 r. przez amerykańską rządową Agencję Żywności i Leków (Food and Drug Administration) był AESOP Robotic System.
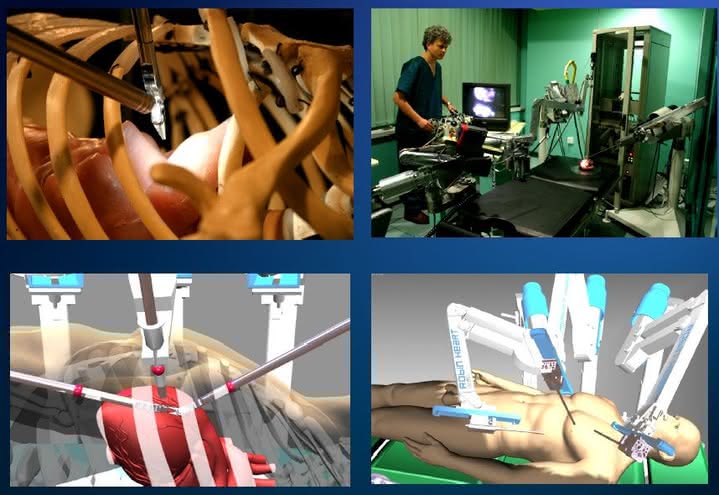
Jego praca polegała na trzymaniu i stabilizacji kamer podczas mało inwazyjnych operacji chirurgicznych. Następny był ZEUS - sterowany, trzyramienny robot wykorzystywany w chirurgii laparoskopowej (4), bardzo podobny do późniejszego robota da Vinci.
We wrześniu 2001 r. przebywający w Nowym Jorku Jacques Marescaux, wykorzystując ZEUS Robotic Surgical System, usunął pęcherzyk żółciowy 68-letniej pacjentce znajdującej się w klinice w Strasburgu.
Chyba najważniejszą zaletą ZEUS-a, jak każdego robota chirurgicznego, była całkowita eliminacja efektu trzęsących się rąk, który dotyka nawet najbardziej doświadczonych i najlepszych chirurgów świata.
Robot jest precyzyjny dzięki zastosowaniu odpowiedniego filtra usuwającego ruchy drgające o częstotliwości ok. 6 Hz, jakie charakteryzują trzęsące się ręce u człowieka. Wspomniany da Vinci (5) stał się słynny już na początku 1998 r., kiedy to francuski zespół dokonał pierwszej na świecie operacji pojedynczego pomostu wieńcowego.
Kilka miesięcy później pomyślnie przeprowadzono plastykę zastawki mitralnej, czyli operację wewnątrz serca. Dla ówczesnej medycyny było to wydarzenie porównywalne do lądowania sondy Pathfinder na powierzchni Marsa w 1997 r.
Cztery ramiona da Vinciego zakończone narzędziami wchodzą w ciało pacjenta przez małe nacięcia powłok ciała. Maszyną steruje chirurg siedzący przy konsoli, wyposażony w system wizyjny, dzięki któremu ogląda operowane miejsce w trójwymiarze, w rozdzielczości HD, naturalnych barwach i 10-krotnym powiększeniu.
Tak zaawansowana technika pozwala na całkowite usunięcie chorych tkanek, zwłaszcza zaatakowanych przez komórki nowotworowe, i obejrzenie trudno dostępnych miejsc, np. w obrębie miednicy mniejszej albo podstawy czaszki.
Inni lekarze mogą obserwować operacje wykonywane za pomocą da Vinciego nawet w miejscach oddalonych o kilka tysięcy kilometrów. Pozwala to na przeprowadzenie zaawansowanych zabiegów chirurgicznych przy wykorzystaniu wiedzy największych autorytetów, bez sprowadzania ich do sali zabiegowej.
Największa grupa wykorzystywana jest do: diagnostyki i rehabilitacji (zwykle pod nadzorem terapeuty, a samodzielnie przez pacjenta głównie w telerehabilitacji), zmiany pozycji i ćwiczeń w łóżku (zrobotyzowane łóżka), poprawy mobilności (zrobotyzowane wózki dla osób niepełnosprawnych i egzoszkielety), opieki (roboty opiekuńcze), pomocy w nauce i pracy (zrobotyzowane miejsca pracy czy zrobotyzowane pomieszczenia), a także terapii w części zaburzeń poznawczych (roboty terapeutyczne dla dzieci i osób w podeszłym wieku).
Bioroboty - grupa robotów stworzonych w celu naśladowania ludzi i zwierząt, którą wykorzystujemy w celach poznawczych. Przykładem jest japoński robot edukacyjny służący przyszłym lekarzom do ćwiczenia operacji. Roboty zastępujące asystenta w czasie operacji - główne ich zastosowanie dotyczy możliwości sterowania przez chirurga położeniem robotycznej kamery, która zapewnia dobre "widzenie" operowanych miejsc.
Jest i polski robot
Historię robotyki medycznej w Polsce rozpoczęli w 2000 r. naukowcy z zabrzańskiej Fundacji Rozwoju Kardiochirurgii, opracowując prototypową rodzinę robotów RobinHeart (6). Mają one segmentową strukturę umożliwiającą zestawienie odpowiedniego sprzętu do różnych operacji.
Powstały modele: RobinHeart 0, RobinHeart 1 - z niezależną podstawą i sterowany komputerem przemysłowym; RobinHeart 2 - mocowany do stołu operacyjnego, mający dwa ramiona, na których można zamontować narzędzia chirurgiczne lub tor wizyjny z kamerą endoskopową; RobinHeart mc2 oraz RobinHeart Vision służący do sterowania endoskopem.
Pomysłodawcą, koordynatorem, twórcą założeń, planowania operacji i wielu rozwiązań mechatronicznych projektu polskiego robota chirurgicznego RobinHeart jest od 2000 r. dr hab. Zbigniew Nawrat. Wraz z nieżyjącym już prof. Zbigniewem Religą był ojcem chrzestnym wszystkich prac, jakie realizują specjaliści z Zabrza w porozumieniu z ośrodkami akademickimi i instytutami badawczymi.
Grupa konstruktorów, elektroników, informatyków i mechaników, którzy pracowali nad RobinHeart, na bieżąco konsultowała się z zespołem lekarskim, by określić wszelkie poprawki, jakie należy do niego wprowadzić.
"W styczniu 2009 r. w Centrum Medycyny Doświadczalnej Śląskiego Uniwersytetu Medycznego w Katowicach, podczas zabiegów na zwierzętach, robot bez problemu wykonał wszystkie powierzone mu zadania. Obecnie trwa wyrabianie dla niego certyfikatów.
Gdy znajdziemy sponsorów, trafi do seryjnej produkcji" - mówił Zbigniew Nawrat z Fundacji Rozwoju Kardiochirurgii w Zabrzu. Polska konstrukcja ma wiele cech wspólnych z amerykańskim da Vinci - umożliwia generowanie obrazu 3D w jakości HD, eliminuje drżenie rąk, a narzędzia przenikają do wnętrza pacjenta teleskopowo.
RobinHeart nie jest natomiast sterowany specjalnymi joystickami jak da Vinci, lecz przyciskami. Jedno ramię polskiego robota-chirurga jest w stanie dzierżyć aż dwa narzędzia, które na dodatek można w dowolnym momencie wyjąć, by np. używać ich manualnie.
Niestety, przyszłość pierwszego polskiego robota-chirurga pozostaje bardzo niepewna. Jak na razie istnieje tylko jeden egzemplarz mc2, który nie wykonał jeszcze żadnej operacji na żywym pacjencie. Powód? Brakuje inwestorów.
Dr Nawrat szuka ich od lat, ale do wdrożenia robotów RobinHeart do polskich szpitali potrzeba ok. 40 mln zł. W grudniu ub. roku zaprezentowano natomiast prototyp lekkiego przenośnego robota toru wizyjnego do szerokiego zastosowania klinicznego: RobinHeart PortVisionAble.
Jego budowę sfinansowano ze środków Narodowego Centrum Badań i Rozwoju, funduszy Fundacji Rozwoju Kardiochirurgii i wielu sponsorów. W tym roku mają powstać trzy modele urządzenia. Jeśli Komisja Etyczna zgodzi się na użycie ich w eksperymencie klinicznym, będą testowane w warunkach szpitalnych.
Nie tylko chirurgia
Na początku wspomnieliśmy o robotach pracujących z dziećmi w szpitalu oraz pobierających krew. Medycyna może znaleźć dla tych maszyn więcej zastosowań "społecznych".
Przykładem jest zrobotyzowany logopeda Bandit stworzony na University of Southern Kalifornia, przeznaczony do wspierania terapii stosowanej wobec dzieci z autyzmem. Wyglądem przypomina zabawkę, co ma ułatwić nawiązywanie kontaktu z pacjentami.
W jego "oczach" usytuowano dwie kamery, a dzięki zamontowanym czujnikom podczerwieni robot, poruszający się na dwóch kołach, potrafi ustalić położenie dziecka i podjąć odpowiednie działania.
Standardowo próbuje najpierw zbliżać się do małego pacjenta, jednak gdy on ucieka, zatrzymuje się i zachęca go gestami do podejścia.
Przeważnie dzieci podchodzą i nawiązują z robotem więź dzięki jego umiejętności do okazywania emocji "mimiką twarzy".
Pozwala to na wciągnięcie dzieci do zabawy, zaś obecność robota ułatwia także interakcje społeczne, takie jak chociażby rozmowa. Kamery robota pozwalają ponadto na nagrywanie zachowania dziecka, wspomagając terapię prowadzoną przez lekarza.
Roboty rehabilitacyjne zapewniające dokładność i powtarzalność umożliwiają wykonywanie ćwiczeń z pacjentami, przy mniejszym zaangażowaniu terapeutów, pozwalając na zmniejszenie kosztów i zwiększenie liczby osób poddanych leczeniu (za jedną z najbardziej zaawansowanych form robota rehabilitacyjnego uważa się egzoszkielet wspomagany).
Ponadto nieosiągalna dla człowieka precyzja pozwala na skrócenie czasu rehabilitacji dzięki większej efektywności działań. Korzystanie z robotów rehabilitacyjnych wymaga jednak nadzoru terapeutów w celu zachowania bezpieczeństwa. Pacjenci często nie zgłaszają bowiem zbyt dużego bólu podczas zajęć, będąc w błędnym przekonaniu, że np. większa dawka ćwiczeń to szybsze efekty.
Nadmierne poczucie bólu zostałoby prawdopodobnie szybko zauważone przez osobę prowadzącą tradycyjną terapię, tak samo jak zbyt łatwe ćwiczenia. Konieczne jest także umożliwienie awaryjnego przerwania rehabilitacji z wykorzystaniem robota podczas np. błędnego działania algorytmu nim sterującego.
Robot Clara (7) stworzony przez USC Interaction Lab jest zrobotyzowaną pielęgniarką. Przemieszcza się po wcześniej zadanych trasach, wykrywając przeszkody. Pacjenci rozpoznawani są przez skanowanie kodów umieszczonych przy łóżkach. Robot wyświetla wcześniej nagrane instrukcje dotyczące ćwiczeń rehabilitacyjnych.
Komunikacja w celach diagnostycznych z pacjentem odbywa się poprzez odpowiedzi "tak" lub "nie". Robot przeznaczony jest dla osób po zabiegach kardiologicznych, u których konieczne jest wykonywanie ćwiczeń spirometrycznych nawet do 10 razy na godzinę przez kilka dni. W Polsce również powstał robot ułatwiający rehabilitację.
Zaprojektował go Michał Mikulski, pracownik Zakładu Sterowania i Robotyki Politechniki Śląskiej w Gliwicach. Prototypem był egzoszkielet - urządzenie zakładane na rękę pacjenta, zdolne do analizy i usprawniania pracy mięśni. Mogłoby ono jednak służyć tylko jednemu pacjentowi i byłoby bardzo drogie.
Naukowcy postanowili więc stworzyć tańszego robota stacjonarnego, mogącego pomagać w rehabilitacji dowolnej części ciała. Przy całym entuzjazmie do robotyki warto jednak pamiętać, że korzystanie z robotów w medycynie nie samymi różami jest usłane. W chirurgii np. wiąże się ze sporymi kosztami.
Wykonanie zabiegu z użyciem znajdującego się w Polsce systemu da Vinci kosztuje ok. 15-30 tys. zł, a po dziesięciu zabiegach trzeba kupić nowy zestaw narzędzi. NFZ nie refunduje operacji przeprowadzanych za pomocą tego sprzętu, wartego ok. 9 mln zł.
Jego wadą jest również przedłużanie czasu potrzebnego na zabieg, przez co pacjent musi dłużej przebywać pod narkozą oraz być podłączony do krążenia pozaustrojowego (w przypadku operacji na sercu).