Nowe techniki obrazowania medycznego

Dziś arsenał narzędzi do obrazowania medycznego jest tak bogaty i różnorodny, że w niedługim artykule trudno nawet tylko wyliczyć wszystkie techniki. W dodatku lista jest wciąż aktualizowana i wzbogacana o nowe pozycje, bo lekarze i badacze już dawno nie zadowalają się odpowiedzią na pytanie "co jest w środku". Chcą wiedzieć dokładnie, co tam się dzieje, co może się dziać, jak skuteczne jest leczenie i co to wszystko razem znaczy.
Od lepszego kontrastu po obserwację zmian na żywo
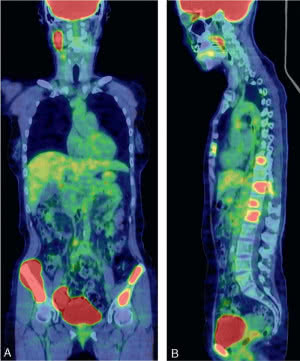
Powszechne jest np. stosowanie w obrazowaniu i diagnostyce biomarkerów. Są to wskaźniki konkretnego stanu chorobowego, oferujące możliwość zwiększenia skuteczności w rozwoju leków. Jako obrazową ocenę działania leków stosowanych w leczeniu nowotworów wykorzystuje się choćby wychwytywanie fluorodeoksyglukozy 18F-FDG przez aktywne komórki rakowe, widoczne w skanach pozytonowej tomografii emisyjnej PET (2). Kolejne skany po aplikacji tego biomarkera badają regresję nowotworu.
Samego guza wykryć można np. przez obrazowanie ukierunkowane, w którym pacjentowi aplikuje się środek kontrastowy (pozwalający lepiej widzieć obszar choroby na skanie) z cząsteczką adhezyjną nastawioną na żądany obszar. Po wstrzyknięciu do krwiobiegu, specyficzne dla danego miejsca cząsteczki adhezyjne - takie jak przeciwciała monoklonalne, peptydy, koproteiny lub polisacharydy - przyklejają się do guza. Ten zaś jest wtedy dobrze widoczny i oglądany na skanach MRI, PET/CT lub USG.
Obrazowanie może być też wspomagane nanocząsteczkami. W skanach MRI wykorzystuje się nanoskalowe środki kontrastowe, wykonane z materiałów żelaznych lub gadolinowych, które rezonują pod wpływem energii pola magnetycznego, zamknięte w węglowych nanorurkach.
Sanjiv Gambhir, dyrektor Stanford Center for Cancer Nanotechnology Excellence (CCNE), finansowanego przez NCI, czyli amerykański Narodowy Instytut Raka, opracował nanoskalowe kropki kwantowe, które wykorzystują reakcję chemiczną do generowania własnego światła w organizmie i sygnalizowania lokalizacji guza.
Przed wykonaniem medycznego badania obrazowego - np. pozytonowej tomografii emisyjnej (PET) lub tomografii emisyjnej pojedynczych fotonów (SPECT) - pacjentowi wstrzykuje się też, albo połyka on, materiały radioaktywne, zwane radiotrackerami lub radiofarmaceutykami.
Podczas skanowania kamera kierowana jest na obszar, w którym koncentruje się materiał radioaktywny, pokazując lekarzowi, w czym problem. Tego typu obrazowanie jądrowe staje się szczególnie pomocne przy diagnozowaniu chorób tarczycy, pęcherzyka żółciowego, serca, raka i choroby Alzheimera.
Skanowanie PET nie jest całkiem nową techniką, ale w ostatnich latach zyskało na znaczeniu - zwłaszcza że zostało połączone w jednym urządzeniu z tomografią komputerową. W przeciwieństwie do wielu innych technologii obrazowania, skany PET nie są przeznaczone do badania organów i tkanek. Zamiast tego mogą obrazować funkcje biologiczne, takie jak przepływ krwi czy metabolizm glukozy. Dają lekarzowi szerszy wgląd w stan zdrowia danej osoby.
W "Journal of Nuclear Medicine" z kwietnia 2019 r. naukowcy opisali wykorzystujący PET sposób na lepsze przewidywanie postępu choroby Alzheimera, z zastosowaniem tzw. obrazowania amyloidowego. Do tej pory takie badania przeprowadzano dopiero w trakcie autopsji zmarłej osoby.
Wkraczają algorytmy
Jeszcze większą nowością niż kolejne techniki skanów i prześwietleń w obrazowaniu organizmu jest semantyczna analiza danych w systemach informacji medycznej. Systemy takie mogą być oparte na metodach analizy strukturalnej obrazowania medycznego i zmierzają do automatycznej interpretacji obrazów.
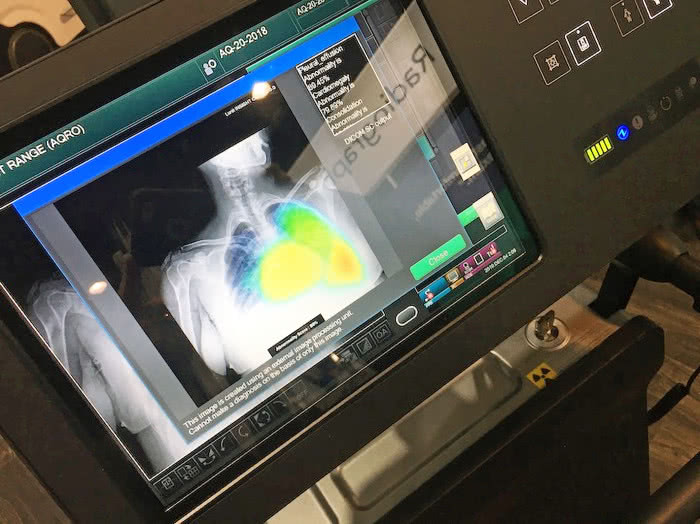
Coraz częściej słyszymy o badaniach, w których systemy oparte na sztucznej inteligencji z większą statystyczną dokładnością niż specjaliści-lekarze diagnozują pacjentów na podstawie skanów oraz obrazów rentgenowskich lub uzyskanych za pomocą innych technik (3).
Raport Data Bridge Market Research z kwietnia 2019 r. szacuje, że wartość rynku sztucznej inteligencji na rynku obrazowania medycznego wzrośnie z 21,5 mld dolarów w 2018 r. do 265 mld dolarów w 2026 r.
Znamy już sporo przykładów bardzo udanych zastosowań AI. Technologia związana z DeepMind firmy Google potrafi odczytywać skany 3D siatkówki i diagnozować pięćdziesiąt różnych problemów okulistycznych z 99-procentową dokładnością. Co więcej, może ona nie tylko automatycznie wykrywać choroby oczu, ale także wskazywać pacjentów najbardziej potrzebujących pilnej opieki.
Firma iCAD opracowała rozwiązanie do cyfrowej tomosyntezy piersi (DBT) o nazwie ProFound AI, które pomaga radiologom samodzielnie przeglądać każdą warstwę tkanki i tym samym wcześniej (o 8%) wykrywać nowotwory. Skraca to czas poświęcany przez radiologów na czytanie skanów piersi średnio o ponad 50%.
Firmy Siemens Healthineers oraz Intel współpracują ze sobą w projekcie, którego celem jest wykorzystanie sztucznej inteligencji do poprawy diagnostyki MRI serca. Obecnie kardiolodzy muszą ręcznie segmentować wiele różnych części serca w swoich badaniach obrazowych - co bywa dość czasochłonne. Technologia błyskawicznej segmentacji z wykorzystaniem sztucznej inteligencji umożliwia specjalistom bezpieczne oglądanie większej liczby pacjentów.
Firma GE Healthcare wprowadziła nową technologię obrazowania medycznego w postaci radiologicznego systemu ultrasonograficznego LOGIQ E10, który jest wspomagany przez sztuczną inteligencję służącą do szybkiego przechwytywania danych i rekonstrukcji obrazów.
Cyfrowy system wykorzystuje zamkniętą łączność i zaawansowane algorytmy, które zapewniają 48-krotnie większą przepustowość danych i dziesięciokrotnie większą moc obliczeniową niż poprzednie systemy. Funkcja łączności w chmurze nosi nazwę Tricefy i umożliwia lekarzom natychmiastowe dzielenie się ze swoimi współpracownikami i pacjentami różnymi ważnymi informacjami medycznymi, takimi jak obrazy, informacje diagnostyczne i dokumentacja medyczna.
Z kolei technologia Center for Advanced Intelligence Project, opracowana przez japońskie Centrum Zaawansowanej Inteligencji RIKEN, z powodzeniem radzi sobie w rozpoznawaniu zmian rakowych na zdjęciach, bez adnotacji stosowanych przez lekarzy. AI identyfikuje tu cechy istotne dla prognozowania nowotworów, które nie zostały wcześniej zauważone przez patologów, co prowadzi do większej dokładności w zakresie rozpoznawania nawrotów raka prostaty w porównaniu z diagnozami opartymi na tradycyjnych metodach.
Według dr. Yoichiro Yamamoto, głównego autora pracy opublikowanej w "Nature Communications", "technologia ta może przyczynić się do rozwoju spersonalizowanej medycyny, umożliwiając bardzo dokładne przewidywanie nawrotów raka przez pozyskiwanie z obrazów nowej wiedzy".
Więcej wygody i komfortu
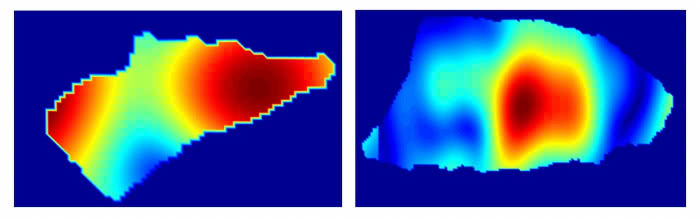
Specjaliści są zdania, że przyszłością jest upowszechnienie technik obrazowania medycznego oraz stosowanie ich w nowych miejscach i sytuacjach, a także w urządzeniach przenośnych (4).
Wyobraźmy sobie cyfrowy detektor obrazu wbudowany w nosze w karetce pogotowia. W krytycznych momentach, jeszcze przed dotarciem do szpitala, personel ratunkowy wykonuje zdjęcia organów pacjenta, które przesyła bezprzewodowo do szpitala, ułatwiając personelowi SOR-u rozpoczęcie leczenia natychmiast po przybyciu, lub szybkie konsultacje jeszcze w drodze.
Technologie obrazujące mogą być też umieszczone w szpitalnym łóżku, wózku inwalidzkim, a nawet w ubraniu, co pozwala na wykonywanie zdjęć rentgenowskich przy minimalnych niedogodnościach dla pacjenta. Urządzenia takie uwalniają przy okazji zasoby szpitalne, eliminując konieczność transportu chorych do miejsc diagnostyki.
W nurcie tym utrzymuje się lekki przenośny skaner magnetoencefalograficzny mózgu, który został opracowany przez naukowców z londyńskiego University College. Może być noszony jak kask, mierząc aktywność mózgu, gdy ludzie wykonują naturalne ruchy, takie jak kiwanie głową, rozciąganie, picie herbaty, a nawet grają w ping ponga. Da się go stosować np. u chorych na epilepsję.
Inny przykład przenośnego obrazowania medycznego to rękawica MRI, wprowadzona przez New York University School of Medicine, zapewniająca wyraźny, stały obraz ruchomych stawów i ścięgien. Uzyskane dzięki niej informacje mogą posłużyć do stworzenia wyraźnej mapy anatomii ręki, pomagając praktycznie we wszystkim, począwszy od operacji, a skończywszy na projektowaniu dokładniejszej protetyki.
Komfort stosowania to nie tylko przenośność urządzeń. Dla wielu osób rezonans magnetyczny jest niezbyt przyjemnym doświadczeniem. W standardowych badaniach MRI osoba wsuwa się do wąskiej rury i musi tam pozostać przez cały czas trwania badania.
Dla osób z klaustrofobią to trudne do zniesienia. Stąd pomysł na urządzenia zwane Open MR. Nie są one zamknięte po bokach, choć zdaniem ekspertów mogą być przez to nieco mniej dokładne. Dostępne są też nowe aparaty MRI, tak samo dokładne jak tradycyjne, ale znacznie krótsze, więc nigdy niezamykające w sobie całego pacjenta.
Komfort pacjentów z poparzeniami może znacząco zwiększyć również ultradźwiękowa maszyna laserowa do obrazowania medycznego, zaprezentowana przez MIT pod koniec 2019 r., która zapewnia bezdotykową diagnostykę. Fala laserowa przenika do stosunkowo wodnistego środowiska ludzkiej skóry i dalej w tkanki znajdujące się poniżej. Osiąga się to poprzez podgrzewanie wody oraz powodowanie jej rozszerzania się i kurczenia w celu wytworzenia fal dźwiękowych.
Drugi laser odbiera te fale i tworzy obraz. Pacjenci nic nie czują, a ponieważ długość laserowych fal wynosi zaledwie 1550 nanometrów, są one bezpieczne dla ludzkiej skóry, a przy okazji łatwo absorbowane przez wodę.
Pomaga chirurgom lub ich zastępuje
Innowacjom nie ma końca. Dzięki niedawno zademonstrowanego wynalazkowi opracowanemu na Uniwersytecie Waterloo możliwe wydaje się precyzyjne, w stopniu dotychczas niespotykanym, lokalizowanie krawędzi guzów podczas operacji ich usuwania.
Nowa technika obrazowania wykorzystuje różnice w sposobach, w jaki światło z laserów wchodzi w interakcję z nowotworowymi i zdrowymi tkankami, umożliwiając odróżnienie ich w czasie rzeczywistym i bez kontaktu fizycznego.
"W trakcie operacji chirurg zobaczy dokładnie, co i ile trzeba ciąć", wyjaśnia w "Scientific Reports" Parsin Haji Reza, profesor inżynierii systemowej, prowadzący ten projekt.
Obecnie lekarze opierają się przede wszystkim na przedoperacyjnych obrazach MRI, tomografii komputerowej, doświadczeniu i oględzinach w celu określenia granicy guza podczas operacji. Próbki tkanek są następnie wysyłane do laboratoriów w celu przeprowadzenia badań, przy czym czas oczekiwania na wyniki wynosi wiele dni lub tygodni, po których dopiero można stwierdzić, czy guz został całkowicie usunięty.
Wkrótce testy obrazowe mogą stać się kluczowym elementem niektórych procedur medycznych. Podczas minimalnie inwazyjnych zabiegów chirurgicznych obrazowanie pozwoli chirurgom lepiej widzieć wnętrze ciała, usprawni leczenie - i zminimalizuje komplikacje.
Niskoinwazyjna chirurgia i nowe technologie obrazowania rozwijają się zresztą równolegle. Nie trzeba dodawać, że w wielu przypadkach dokładne, zaawansowane obrazowanie może po prostu zastąpić chirurgię, bo nie trzeba będzie kroić, aby zobaczyć wszystko, co trzeba obejrzeć we wnętrzu pacjenta.
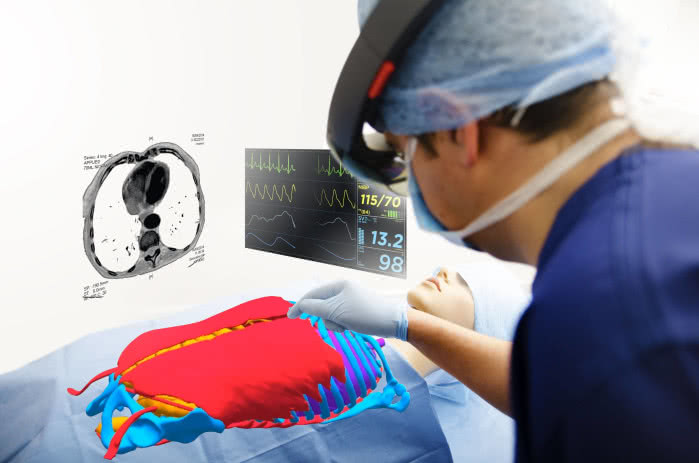
Innym przyszłościowym obszarem jest tzw. chirurgia 3D (5). W tradycyjnym podejściu chirurdzy polegają na wykonywanych przed operacją płaskich zdjęciach rentgenowskich ukazujących obszary dotknięte chorobą, a także na technikach inwazyjnych w celu zlokalizowania trudno dostępnych guzów lub uszkodzonych organów na sali operacyjnej.
Tymczasem w chirurgii trójwymiarowej wykorzystuje się tomografię komputerową, rezonans magnetyczny i kamery diodowe emitujące światło do tworzenia trójwymiarowych obrazów pola operacyjnego w czasie rzeczywistym oraz precyzyjnej lokalizacji zmian chorobowych.
Chirurgia tego rodzaju ma wiele zastosowań i jest szczególnie przydatna dla neurochirurgów w ocenie przedoperacyjnej guzów mózgu - chirurdzy są dzięki niej w stanie dokładniej usuwać guzy bez powodowania nowych urazów delikatnych struktur. Technologie rzeczywistości rozszerzonej, takie jak EchoPixel True 3D, umożliwiają dziś radiologom lub lekarzom robienie "plastrów" zdjęć MRI w celu stworzenia trójwymiarowego obrazu, który można potem badać za pomocą okularów 3D, gogli VR, a nawet drukować na drukarce 3D z wykorzystaniem specjalnego tworzywa sztucznego.
Zdaniem specjalistów, w ciągu najbliższych dwudziestu lat technologia obrazowania skoncentruje się na poziomie molekularnym i komórkowym. Zamiast patrzeć tylko na anatomię, jak to przeważnie robiono do tej pory, lekarze będą obserwować metabolizm i fizjologię.
Skanowanie PET uważane jest za pierwszy krok w tym kierunku. Upowszechniać się będzie też łączenie wielu metod. Istnieją już prototypowe skanery PET/MRI, a mówi się o urządzeniach kombinowanych TK/MRI. Jeśli dodać do tego nowoczesne techniki prezentacji obrazu, mieszaną rzeczywistość i zanurzanie w środowisku VR, to praca przyszłych lekarzy może stać się naprawdę niezwykłym doświadczeniem.
Mirosław Usidus