Nanomedycyna pokonuje kolejne granice

System biomedyczny opracowany przez grupę naukowców ze szwajcarskiego Państwowego Instytutu Technologicznego w Zurichu napędzany jest zewnętrznym polem magnetycznym. Małe urządzenia mają szerokość zbliżoną do czterokrotnej średnicy ludzkiego włosa i są złożone z kilku części.
Proces składania tych mechanicznych i elektronicznych komponentów jest bardzo podobny do tego, jaki stosuje się przy budowie mikroprocesorów.
Urządzenie w polu magnetycznym zachowuje się jak igła kompasu - dzięki wykorzystaniu tej własności można nim sterować: "czubek" robota ma znak "plus", podczas gdy jego koniec ma ładunek ujemny.
Przetestowany w warunkach laboratoryjnych okazał się bardzo dobrze sterowalnym mechanizmem, pomimo iż poruszał się w niezwykle małych kanalikach - o szerokości zaledwie 10 grubości włosa.
Bakteriobot zamiast chemioterapii
Za prekursora nanotechnologii uchodzi słynny fizyk, Richard Feynman. Jego wykład z 1959 r. zatytułowany "Tam na dole jest mnóstwo miejsca" nakreślił wizję przyszłości, świata manipulacji mikroobiektami. Dziś ta wizja zaczyna przybierać realne kształty. Postęp w mikro- i nanoinżynierii medycznej skutkuje tworzeniem projektów różnych robotów, które pewnego dnia umożliwią medycynie małoinwazyjnej osiągnięcie nowego poziomu.
Te mikro- i nanoroboty będą w stanie dotrzeć do konkretnego obszaru ciała, zapewnić w tym miejscu wymagane leczenie, monitorować jego efekty, a na zakończenie ulegną degradacji, w sposób niepowodujący działań niepożądanych. Najlepiej byłoby, gdyby wszystkie te czynności były zautomatyzowane, ale mogłyby być także przeprowadzone pod bezpośrednim nadzorem i kontrolą użytkownika z zewnątrz.
Zespół pod przewodnictwem prof. Peera Fischera z Instytutu Inteligentnych Systemów Maxa Plancka w Stuttgarcie jest na dobrej drodze do opracowania mikroskopijnych robotów, które będą potrafiły podróżować w płynach naszego organizmu. Mają kształt ząbkowanych naczyń w formie muszli (2).
Do nawigacji będą wykorzystywały zewnętrzne pole magnetyczne. Pomysł badaczy wzorowany jest na rozwiązaniu znanym z natury - niewielkie małże, przegrzebki oraz skalopki poruszają się, odpowiednio zamykając i otwierając muszle. Jak podała agencja Reuters, specjaliści z Korei Południowej opracowali pierwszego nanorobota, który potrafi wykryć komórki raka i je zniszczyć przy użyciu chemioterapeutyków.
Na razie przetestowano go na myszach. Nanorobot jest bakteriobotem, gdyż wykorzystano w nim zmodyfikowane genetycznie bakterie salmonelli. Kierujący badaniami Park JongOh z Narodowego Uniwersytetu Chonnam zmienił je za pomocą manipulacji genetycznych z tworów szkodliwych dla organizmu na użyteczne czujniki wykrywające substancje chemiczne wydzielane przez komórki rakowe.
Koreański bakteriobot po wprowadzeniu do organizmu przenika do komórek rakowych, kierując się wysyłanymi przez nie sygnałami chemicznymi. W jego środku znajdują się mikrokapsułki z chemioterapeutykami, które są uwalniane, gdy tylko bakteria dotrze do komórek nowotworowych. Chemioterapeutyki atakują je i niszczą - nie naruszając przy tym zdrowych tkanek otaczających guza. Gdyby
udało się przenieść ten mechanizm do organizmu ludzkiego, powstałaby wspaniała alternatywa dla uciążliwej chemioterapii, w której leki podawane są w potężnych dawkach, co jest toksyczne nie tylko dla komórek rakowych, ale również i zdrowych. Bakterioboty uwalniają znacznie mniejsze dawki leków i atakują nimi bezpośrednio guza, dzięki czemu ich działanie może być znacznie bardziej skuteczne.
Nanomotory szaleją w komórkach
Kwestią kluczową dla nanobotów są techniki napędowe. Spalanie jakichkolwiek paliw w ludzkim organizmie raczej nie wchodzi w grę, aby nie doszło do zatruć i zanieczyszczeń w płynach ustrojowych oraz komórkach. Jak dotąd rozważano kilka sposobów wprawiania robotów w ruch na odległość.
Najczęściej brano pod uwagę zastosowanie pola magnetycznego, gdyż nie wymaga ono specjalnych właściwości środowiska, w którym miałby poruszać się robot (jak przejrzystość czy przewodnictwo).
Taki sposób pozwala na precyzyjne przesuwanie obiektów magnetycznych w kierunku konkretnych miejsc, a pole magnetyczne samo w sobie spełnia warunki biozgodności, nawet w przypadku jego stosunkowo dużego natężenia.
Badaczom z Uniwersytetu Teksaskiego w Austin udało się skonstruować najmniejszy, najszybszy i najdłużej pracujący nanosilniczek (3), jaki znamy. Jego rozmiar nie przekracza jednego mikrometra. Osiąga 18 tys. obrotów na minutę i pracuje bez przerwy nawet do 15 godzin.
Zbudowany przez zespół pod kierownictwem profesor Donglei Fan, jest konstrukcją "niebiologiczną". Potrafi szybko mieszać i pompować substancje biologiczne potrzebne organizmowi na poziomie komórkowym. Jest także w stanie poruszać się w środowisku ciekłym, co jest istotne w medycznych zastosowaniach, bo właśnie o takich się mówi w odniesieniu do tego nanosilnika.
Urządzenie zostało zbudowane na podstawie opatentowanej przez profesor Fan technologii wykorzystującej zmiany pola elektrycznego przy przepływach prądów stałych i zmiennych. Zmiany pola służą również do napędzania silniczka, przemieszczania go oraz kontroli nad procesami wyzwalającymi substancje czynne w organizmie.
Naukowcy z uniwersytetu Penn State zdołali umieścić nanomotory w żywych ludzkich komórkach i sterować ich ruchami za pomocą fal dźwiękowych o wysokiej częstotliwości oraz magnesów. Taka sztuka nie udała się nikomu wcześniej. Dotychczas "roboty" molekularne demonstrowane były jedynie w próbówkach (in vitro).
Mikroroboty mają długość kilku mikrometrów i wyglądają trochę jak zapałki. Zrobione są z metali: rutenu i złota. Zostały wchłonięte przez komórki rakowe, w których zaczęły się szybko przemieszczać, po skupieniu na nanomotorach fal akustycznych. O ile fale dźwiękowe wykorzystywane są jako "napęd", o tyle siły magnetyczne jako "stery" do kierowania mikrorobotów w określonych kierunkach.
Naukowcy snują wizje wykorzystania minimotorków jako narzędzi transportujących substancje chemiczne w określone miejsca komórki. Mogą również służyć w diagnostyce, w której odpowiednio skonfigurowane robociki zajmą się zbieraniem informacji o sytuacji w komórce, wykrywając zawczasu początkowe zmiany patologiczne.
Odrobina inteligencji
W pracy opublikowanej w listopadzie 2013 r., w czasopiśmie "Advanced Materials", zespół badaczy z Politechniki Federalnej w Zurychu oraz z Uniwersytetu Harvarda (laboratorium Davida Mooneya) wykazał, że w małych robotach może pojawić się dodatkowa inteligencja - odbieranie bodźców oraz uwalnianie substancji do otoczenia - a to poprzez wybór odpowiednich materiałów i metod procesu produkcyjnego.
Uczeni wyposażyli hydrożelowe kapsułki reagujące na światło bliskiej podczerwieni w mikrożele magnetyczne. Do poruszania robotami używany jest system manipulacji magnetycznej, który pozwala na dostarczanie leków czy komórek do konkretnych miejsc.
We wspomnianym artykule naukowcy opisują, jak udało się im stworzyć samoorganizujące się, miękkie "platformy", w ramach których zintegrowane są różne funkcje pozwalające na odgrywanie docelowej roli - dostarczania czynników biologicznych na żądanie. Hydrożele reagujące na bodźce stanowią klasę materiałów, których właściwości fizyko-chemiczne są podobne do właściwości tkanek biologicznych.
Zachodzi w nich odwracalna zmiana objętości w odpowiedzi na różne bodźce (temperatura, pH, siła jonowa itp.). Wykorzystuje się je w inżynierii tkankowej, w celu dostarczania leków oraz komórek, są także pomocne w procesie gojenia się ran. Dwuwarstwowa, hydrożelowa struktura ulega zwinięciu, gdy każda z dwóch warstw zmienia swoją objętość w odpowiedzi na różne bodźce fizyko-chemiczne.
Tworzone przez zespół naukowców mikrostruktury mogą przechodzić z formy zamkniętej w otwartą, gdy ich temperatura przewyższa 40°C. Naukowcy tak zaprojektowali te mikrostruktury, żeby krótka ekspozycja na światło podczerwone wystarczyła do osiągnięcia wymaganej temperatury i zmianę konfiguracji. W ten sposób osoba z zewnątrz może z pewnej odległości na nie wpływać.
Światło w zakresie bliskiej podczerwieni jest w stanie przenikać przez tkanki ciała bez powodowania uszkodzenia. Tak więc da się sterować mikrorobotami w organizmie. Wszystko wygląda niezwykle obiecująco, choć tak naprawdę to wciąż wyłącznie laboratoryjne eksperymenty. Prowadzący je naukowcy widzą cztery główne pola zastosowań minirobotów.
W nauce - zauważono, że w sytuacji kolizji i nacisku małych pojazdów na obiekty we wnętrzu komórki, pojawiają się nigdy dotąd nieobserwowane odruchy komórkowe, co może otworzyć przed nami zupełnie nowe obszary badań. W terapii, ponieważ do poszczególnych części komórki będzie można dostarczać substancje z niespotykaną dotąd dokładnością.
W chirurgii, bowiem wehikuły potrafią przebijać błony komórkowe oraz niszczyć pojedyncze elementy w komórce, co ułatwi operacje chirurgiczne w nanoskali. I wreszcie w diagnostyce, gdyż nasi mali eksploratorzy będą zbierać informacje o kondycji wybranych części komórki, a potem dostarczać je lekarzom.
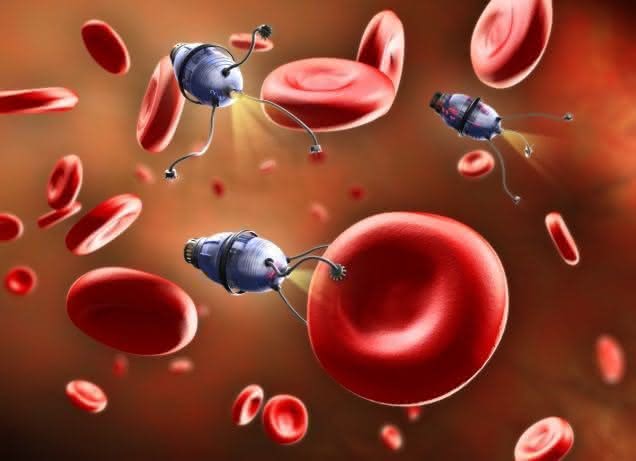
W dalszej przyszłości miniaturowe roboty mogłyby, być może, uzupełniać naturalny system immunologiczny człowieka, "patrolując" wewnątrz systemu krwionośnego (4). Wizje odbudowy zniszczonych komórek od środka i zbliżenia się do nieśmiertelności to wciąż science-fiction, ale same nanoroboty być może już za kilka lat zaczną działalność na szeroką skalę?
Poligon w kształcie żołądka
Innym wątkiem badań i eksperymentów, w skali raczej mikro niż nano, są kapsułki diagnostyczne, które się połyka, po czym eksplorują one nasz organizm, np. nagrywając film. Produkty mające taką właśnie funkcję tworzy izraelska firma Given Imaging, pod nazwą PillCam (5). Firma Philips wyprodukowała z kolei inteligentną, zrobotyzowaną pigułkę iPill.
Umożliwia ona dostarczenie leku dokładnie w pożądane miejsce w organizmie. Wnętrze pigułki o wymiarach 11×26 mm zawiera m.in. układ komunikacji radiowej, mikroprocesor, baterię oraz miniaturową pompę. Dzięki umieszczonym w kapsułce czujnikom, iPill może dokonać pomiaru odczynu pH w celu określenia położenia w układzie pokarmowym, pozwalając na uwolnienie leku w dokładnie ustalonym miejscu.
Istnieje także możliwość dostarczania leku w porcjach, w kilku miejscach układu pokarmowego. Ponadto przewidziano też opcję zdalnego wydania polecenia wstrzymującego dozowanie leku, w przypadku np. wystąpienia skutków ubocznych. Wbudowana bateria pozwala na 48 godzin pracy.
Bardziej zaawansowanym projektem tego typu jest "wąż", wspólne dzieło specjalistów z Francji, Szwajcarii i Hiszpanii. Pacjent połyka kilka kapsułek, które same łączą się w organizmie. Połknięcie takiego finalnego węża w całości byłoby zapewne nie lada wyzwaniem, stąd pomysł, aby wprowadzić go do przełyku w kawałkach.
Powstały w ten sposób wewnątrz ciała wielomodułowy robot wykonuje w nim różne prace. Jeden z elementów jest kamerą, inny zawiera baterię zasilającą dla całego urządzenia, kolejny pobiera próbki. Robot-wąż prześlizguje się po jelitach, realizując program diagnostyczny.
Inżynierowie ze szwajcarskiego ETH, którzy pracują nad projektem, przyznają, że największym problemem jest sprawne i szybkie samozłożenie się robota. Uznali, że w tej chwili najlepsze rozwiązanie stanowi układ łączników magnetycznych. Nie wymaga bowiem dodatkowego zasilania i można go monitować z zewnątrz ciała. Naukowcy zbudowali nawet model żołądka z tworzywa, wypełniony ciekłą substancją imitującą warunki w prawdziwym żołądku (6).
Chemicy z Massachusetts Institute of Technology (MIT) opracowali nanocząsteczki, które mogą wykonywać zadania takie, jak medyczny rezonans magnetyczny oraz obrazowanie fluorescencyjne w sposób równie skuteczny co znane technologie.
Nowa koncepcja może posłużyć do monitorowania na bieżąco produkcji cząsteczek w organizmie, zmian nowotworowych i sprawdzania, czy leki dotarły w miejsce, w którym miały zadziałać.
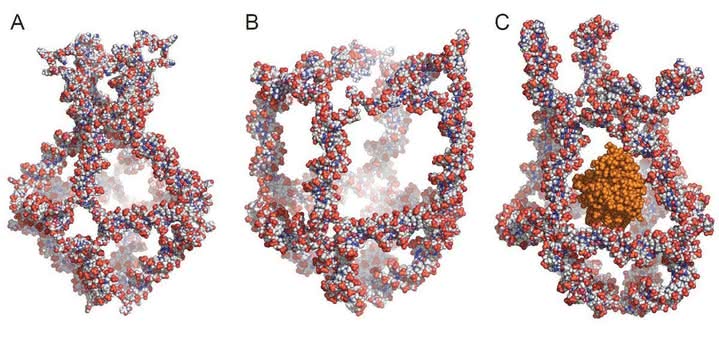
Według opisu opublikowanego w czasopiśmie naukowym "Nature Communications", nanocząsteczki mogą przenosić zarówno sensory służące do techniki rezonansu MRI, jak też fluorescencyjne, które śledziły witaminę C w organizmie myszy. Innym ciekawym projektem było stworzenie nanoklatki złożonej z ośmiu cząsteczek DNA (7), którą naukowcy z Aarhus University ochrzcili nanorobotem kapsułkującym leki.
Nanoklatka składa się samorzutnie, zamykając w swym wnętrzu wybrany związek, np. enzym. Potrafi się również automatycznie otwierać pod wpływem wyższej temperatury wymuszającej zmianę konformacji łańcucha DNA. Nanorobot i podobne jemu struktury DNA mają zostać w przyszłości zastosowane jako niezwykle precyzyjne systemy dostarczania leków do odpowiednich tkanek i narządów.
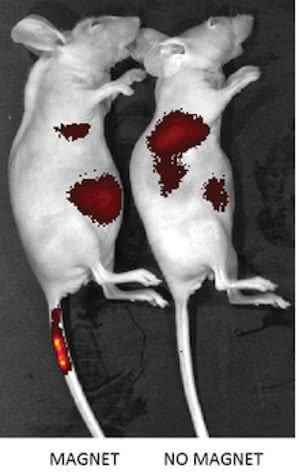
Sterowanie za pomocą magnesu komórkami macierzystymi wydaje się egzotycznym pomysłem, ale nie dla zespołu z uniwersytetów Emory oraz Georgia Tech. Załadowali oni komórki macierzyste nanocząstkami tlenku żelaza i badali ich zachowanie w warunkach laboratoryjnych.
Przykładając pole magnetyczne do ogona szczura, spowodowali nagromadzenie się owych komórek w tym obszarze (8). Naukowcy udowodnili, że można szybko transportować komórki macierzyste do miejsc wymagających natychmiastowej regeneracji, np. przy zawale mięśnia sercowego.
Diamenty w leczeniu nowotworów? Dlaczego nie, ale jedynie w skali nano. Projekt grupy z University of California polegał na połączeniu konwencjonalnego leku doksorubicyny z niekonwencjonalnym jak dotąd nośnikiem, czyli nanodiamentem. Nośnik ten odznacza się biozgodnością, czyli nie jest toksyczny, nie atakuje układu odpornościowego oraz pozwala na dłuższe utrzymywanie się efektywnego stężenia leku w obrębie guza.
Ze względu na dobre wyniki eksperymentalnej terapii glejaka rozważane są połączenia nanodiamentów z innymi lekami. Nie tak dawno uczeni ze wspomnianych uczelni Georgia Tech oraz Emory odkryli, że komórki ssaków ze wszystkich kształtów nanocząstek preferują te o kształcie dysku. Wynika to z faktu, iż do owinięcia błony komórkowej wokół nich potrzebna jest stosunkowo najmniejsza ilość energii.
Czy otwiera to nową erę w "designie" nanobotów? Cały czas mamy do czynienia z zaledwie raczkującą nanotechnologią medyczną. Era leków i metod diagnostycznych opartych na nanocząstkach i nanomateriałach rozpoczęła się dopiero niedawno, dlatego większość projektów wciąż znajduje się na etapie testów.