Analiza elektrograficzna

Wyposażenie niezbędne do przeprowadzenia analizy elektrograficznej jest łatwe do skompletowania. Wystarczy kilka połączonych szeregowo ogniw (zwiększenie napięcia skróci czas reakcji), przewody i metalowa płytka (fot. 1). Z „minusem” baterii łączymy płytkę, a drugi biegun – „plus” – z bolcem, którym będziemy przyciskać badany przedmiot do bibuły. Pozostaje jeszcze tylko sprawdzić układ, np. za pomocą diody LED (fot. 2), i już można przystąpić do eksperymentu.
Zidentyfikujemy niektóre metale za pomocą elektrografii. Do pierwszej próby potrzebny będzie stalowy przedmiot, 5% roztwór żelazicyjanku potasu K3[Fe(CN)6] oraz fragment bibuły filtracyjnej. Bibułę kładziemy na płytce metalowej, zwilżamy przygotowanym roztworem, na niej umieszczamy badany obiekt i przyciskamy go bolcem (fot. 3). Po około 30 sekundach (czas zależy od wielkości napięcia) przerywamy przepływ prądu i zdejmujemy przedmiot z bibuły. Na podłożu widoczny jest wyraźny niebieski ślad (fot. 4).
Plama powstaje w następujący sposób:
1. Badany przedmiot, połączony z dodatnim biegunem baterii, jest anodą.
Przy odpowiedniej wartości napięcia atomy metalu oddają elektrony i w postaci jonów przechodzą do roztworu w bibule:
(+) Fe0 → Fe2+ + 2e–
2. W roztworze jony metalu reagują z odczynnikiem:
3Fe2+ + 2[Fe(CN)6]3– → Fe3[Fe(CN)6]2
Niebieska barwa błękitu Turnbulla jest charakterystyczną reakcją dla jonów żelaza(II).
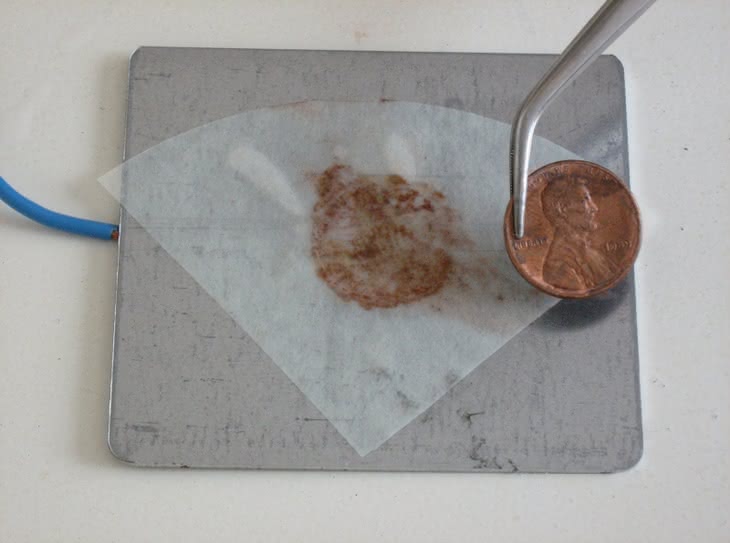
W drugiej próbie potwierdzimy obecność miedzi w starej amerykańskiej jednocentówce. Tym razem bibule nasączamy 5% roztworem żelazocyjanku potasu K4[Fe(CN)6], dalej eksperyment przebiega analogicznie jak podczas pierwszej próby (fot. 5). Dowodem obecności miedzi jest brunatny osad żelazocyjanku tego metalu (fot. 6):
2Cu2+ + [Fe(CN)6]4– → Cu2[Fe(CN)6]↓
Kolejny eksperyment polega na wykryciu ołowiu w kawałku taśmy wykonanej z tego metalu. Użytym elektrolitem jest 2% roztwór chromianu potasu K2CrO4 (fot. 7). Po przerwaniu przepływu prądu pod taśmą znajduje się żółty ślad osadu chromianu ołowiu (fot. 8):
Pb2+ + CrO42–→ PbCrO4↓
Ostatnia próba to potwierdzenie obecności niklu w stopie, z którego wykonana jest moneta o nominale 1 zł. Roztwór elektrolitu zawiera 1% dimetyloglioksymu oraz 5% chlorku amonu NH4Cl (fot. 9). Dowodem obecności niklu w badanej próbce jest różowa barwa kompleksowego połączenia jonów tego metalu (fot. 10):
Znając charakterystyczne reakcje jonów metali można samodzielnie zaprojektować doświadczenie elektrograficzne oraz wykryć te metale w zawierających je stopach.
Zobacz to na filmie: