Zegar jodowy

Potrzebne będą: 1% roztwór jodku potasu KI, 4% kwas solny HCl, 0,1% roztwór tiosiarczanu sodu Na2S2O3, woda utleniona (roztwór nadtlenku wodoru H2O2 o stężeniu 3%) oraz wskaźnik skrobiowy (łyżeczka mąki ziemniaczanej rozpuszczona w 50 cm3 ciepłej wody).
Do zlewki o pojemności 100 cm3 wlewamy 5 cm3 roztworu KI i 5 cm3 kwasu solnego. Z powodu utleniania anionów jodkowych do wolnego pierwiastka zawartość zlewki może lekko ściemnieć. Do naczynia dodajemy 10 cm3 roztworu Na2S2O3 i 1 cm3 wskaźnika skrobiowego. Całość dopełniamy wodą do objętości 50 cm3. Ciecz w zlewce powinna pozostać bezbarwna, ewentualnie lekko mętna (zawiesina skrobi). Teraz dodajemy 5 cm3 wody utlenionej i czekamy na efekt (fotografia 1). Jest on widowiskowy (fotografia 2): przez kilkanaście do kilkudziesięciu sekund nic się nie dzieje, aż nagle, jak za dotknięciem czarodziejskiej różdżki, zawartość zlewki staje się granatowa!
Jakie procesy przebiegły w naczyniu?
1. Powolna reakcja utleniania anionów jodkowych przez nadtlenek wodoru do wolnego jodu:
2. Szybka reakcja między wolnym jodem i tiosiarczanem sodu:
Wolny jod wytworzony w reakcji 1. nie zdąży zabarwić skrobi, ponieważ jest natychmiast redukowany do anionów jodkowych w reakcji 2. Powstające aniony jodkowe reagują z nadtlenkiem wodoru, tworząc I2, który pod wpływem tiosiarczanu sodu ponownie redukuje się do jonów I–. Reakcje zachodzą aż do zużycia tiosiarczanu (wprowadzamy go mniej, niż wynika ze stechiometrii reakcji - jest to warunek konieczny uzyskania efektu zegarowego!). Wtedy dopiero wolny jod powstający w reakcji 1. zabarwia wskaźnik skrobiowy. Dobierając odpowiednio ilości substratów, możemy regulować czas pojawienia się granatowego zabarwienia.
Modyfikując nieco klasyczną reakcję Harcourta uzyskamy ciekawy efekt barwny. Do zestawu odczynników z poprzedniej próby dołączamy 1% roztwór azotanu(V) ołowiu(II) Pb(NO3)2. Można zastąpić go również octanem ołowiu(II) (CH3COO)2Pb (uwaga, obie substancje są trujące!). W zlewce mieszamy roztwory KI, HCl, Na2S2O3, wskaźnik skrobiowy i wodę (w proporcji podanej w poprzednim doświadczeniu), a następnie wlewamy 5 cm3 roztworu soli ołowiu (fotografia 3). Natychmiast wytrąca się złocisty osad jodku ołowiu(II):
Po dodaniu 5 cm3 wody utlenionej (fotografia 4) przez kilkadziesiąt sekund nic się nie dzieje. ale nagle zawartość zlewki zaczyna zmieniać kolor na kawowy (fotografia 5) – jest to efekt nałożenia się barwy żółtej i granatowej. Po około minucie ciecz w zlewce staje się ciemnobrunatna (fotografia 6). Przebiegające reakcje są identyczne jak w poprzedniej próbie, dodatkowo zachodzi rozkład jodku ołowiu(II) przez pod wpływem nadtlenku wodoru:
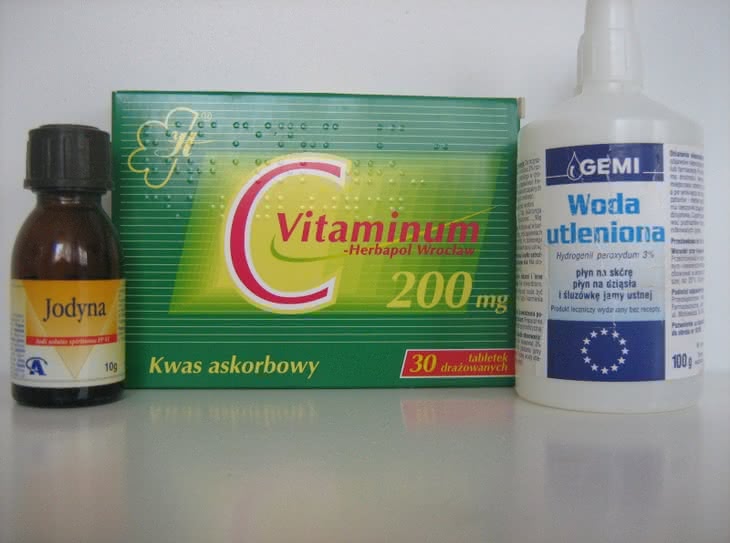
„Zegar jodowy” możemy również wykonać przy użyciu jeszcze łatwiej dostępnych chemikaliów. Wystarczy zawartość domowej apteczki: jodyna, witamina C i woda utleniona (fotografia 7) i oczywiście skrobia w postaci mąki ziemniaczanej (z domowej spiżarni). Do zlewki o pojemności 100 cm3 wlewamy 10 cm3 wody i dodajemy 1 cm3 jodyny (alkoholowy roztwór jodu, można użyć także płynu Lugola – roztworu jodu w jodku potasu). Sporządzamy roztwór witaminy C, rozgniatając jedną tabletkę i rozpuszczając proszek w 20-30 cm3 wody. Roztwór jest nietrwały i musi być świeżo przygotowany przed eksperymentem. Do zlewki z roztworem jodyny dodajemy taką ilość roztworu witaminy C, która zawiera ok. 50 mg kwasu askorbinowego (fotografia 8). Roztwór w zlewce odbarwia się natychmiast. To wolny jod reaguje z wprowadzonym odczynnikiem:
Teraz dodajemy 1 cm3 wskaźnika skrobiowego (fotografia 9) i 10 cm3 wody utlenionej. Po kilkunastu sekundach zawartość zlewki raptownie barwi się na ciemny kolor (fotografia 10).
Zachodzące reakcje są podobne do omówionych. W pierwszym etapie następuje redukcja jodu do anionów jodkowych pod wpływem kwasu askorbinowego. Następnie są one utleniane przez nadtlenek wodoru do wolnego jodu, który znowu redukuje się pod wpływem witaminy C. Po wyczerpaniu całej ilości witaminy wolny jod reaguje wreszcie ze skrobią, barwiąc zawartość zlewki.
Obejrzyjcie to na filmie: