Chemiczny Nobel 2016, czyli jak cząsteczki stały się maszynami

Po latach przyznawania nagród za badania biochemiczne (to co prawda bardzo wyrafinowana chemia, lecz niekojarząca się ogółowi ludzi z obiegowym wizerunkiem uczonego tej specjalności) oraz kontrowersyjnym Noblu z roku 2014 za mikroskopię fluorescencyjną, ostatni werdykt docenił prace typowo chemiczne - stworzenie związków o interesującej budowie i właściwościach, a ponadto mających potencjalnie wielkie zastosowanie w przyszłości. Struktura powstałych molekuł jest tak niespotykana, że ich otrzymanie to wręcz artyzm w dziedzinie syntezy organicznej.
Wizje przyszłości
W roku 1959 Richard Feynman, noblista z roku 1965 i znany popularyzator nauki, wygłosił wykład pt. There is Plenty of Room at the Bottom („Tam na dole jest dużo miejsca”). Podczas prelekcji zasugerował możliwość konstrukcji maszyn oraz komputerów o wielkości porównywalnej z rozmiarami molekuł, a także zapisu informacji przy pomocy pojedynczych atomów. W owym czasie była to czysta SF. Komputery z końca lat 50. ubiegłego wieku zajmowały całe pomieszczenia, a ich moc obliczeniowa była wręcz śmieszna w porównaniu z dzisiejszymi smartfonami. Jednak wystarczyło kilka dziesięcioleci, aby nanotechnologia stała się faktem. Co prawda wciąż dopiero raczkuje, ale już widać, że przed nią jest wielka przyszłość. Wizjonerem (nie tylko w tej dziedzinie) był również Stanisław Lem, który w opowiadaniu „Niezwyciężony” przedstawił zmagania ludzi z rojami mikroskopijnych mechanicznych owadów (nanobotów?). Nagrodzone prace noblistów z roku 2016 okazały się krokiem do realizacji przewidywań sprzed kilkudziesięciu lat.
Łańcuszki…
W połowie ubiegłego wieku chemicy podjęli próby otrzymania skomplikowanych związków, podobnych do spotykanych w organizmach żywych. Jednymi z nich były pierścienie o dużych rozmiarach. Powstawały poprzez połączenie końców długich cząsteczek. Niekiedy zdarzało się jednak, że molekuła przeszła przez środek już utworzonego pierścienia i dopiero wtedy nastąpiło zamknięcie kręgu. W ten sposób powstawał łańcuch złożony z dwóch ogniw. Oczywiście prawdopodobieństwo takiego zdarzenia jest nikłe i chemicy traktowali powstające twory jako swoiste chemiczne kuriozum.
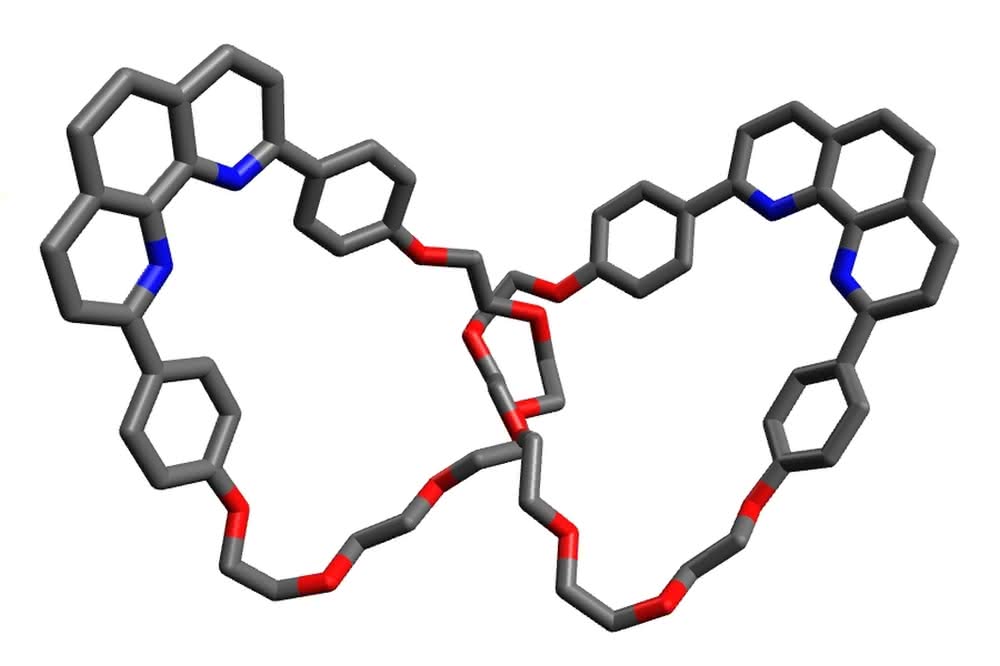
Przypadek spowodował, że odkryto metodę umożliwiającą syntezę tego typu związków z wysoką wydajnością. W roku 1983 Jean-Pierre Sauvage zajmował się reakcjami, w których używał jonów miedzi oraz pewnych połączeń organicznych. W jednej z nich stwierdził tworzenie się dużych ilości nowego związku. W otrzymanej substancji poszczególne części układu nie były połączone żadnym wiązaniem chemicznym pomiędzy atomami, a cały układ trwał tylko dzięki mechanicznemu spleceniu jego składników. Chemicy nazwali połączenie pomiędzy tworzącymi układ molekułami wiązaniem mechanicznym lub topologicznym (topologia to dział matematyki zajmujący się badaniem pewnych własności figur). Same zaś związki nazwano katenanami (z łac. catena - łańcuch) (1). [katenan] Stosując pomysłowe „sztuczki”, oparte na schemacie opisanym w ramce „Synteza katenanu”, zespoły kierowane przez Sauvage’a oraz Frasera Stoddarta uzyskały łańcuchy składające się nawet z siedmiu ogniw oraz pierścienie posplatane ze sobą w rozmaity sposób. W roku 1994 powstał olimpiadan z pięciu okręgów złączonych jak w symbolu ruchu olimpijskiego. W tym samym roku Sauvage doniósł o syntezie katenanu, w którym jeden z pierścieni obracał się w kontrolowany sposób pod wpływem zmian potencjału elektrycznego (np. podczas reakcji z innymi cząsteczkami czy zmiany odczynu roztworu). Pierwszy krok w stronę maszyn molekularnych został zrobiony.
Synteza katenanu
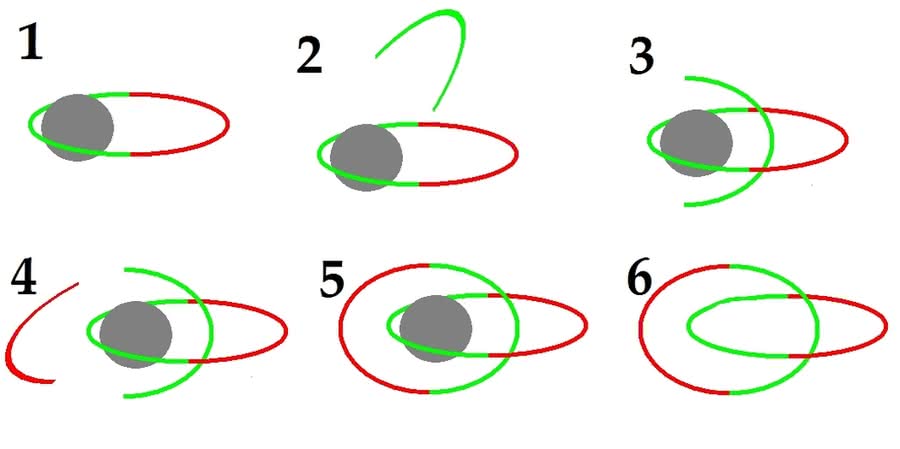
- W pierścieniu powstałym z dwóch cząsteczek lokuje się jon metalu przyciągany przez fragment molekuły (w kolorze zielonym).
- Do kompleksu zbliża się inna cząsteczka wykazująca powinowactwo do metalu, …
- …a następnie przechodzi przez wnętrze pierścienia.
- Do końców tej cząsteczki zbliża się molekuła stanowiąca drugą część pierścienia…
- …i reagują z nią, zamykając krąg.
- Po usunięciu jonu metalu powstaje łańcuch złożony z dwóch ogniw.
…przełączniki…
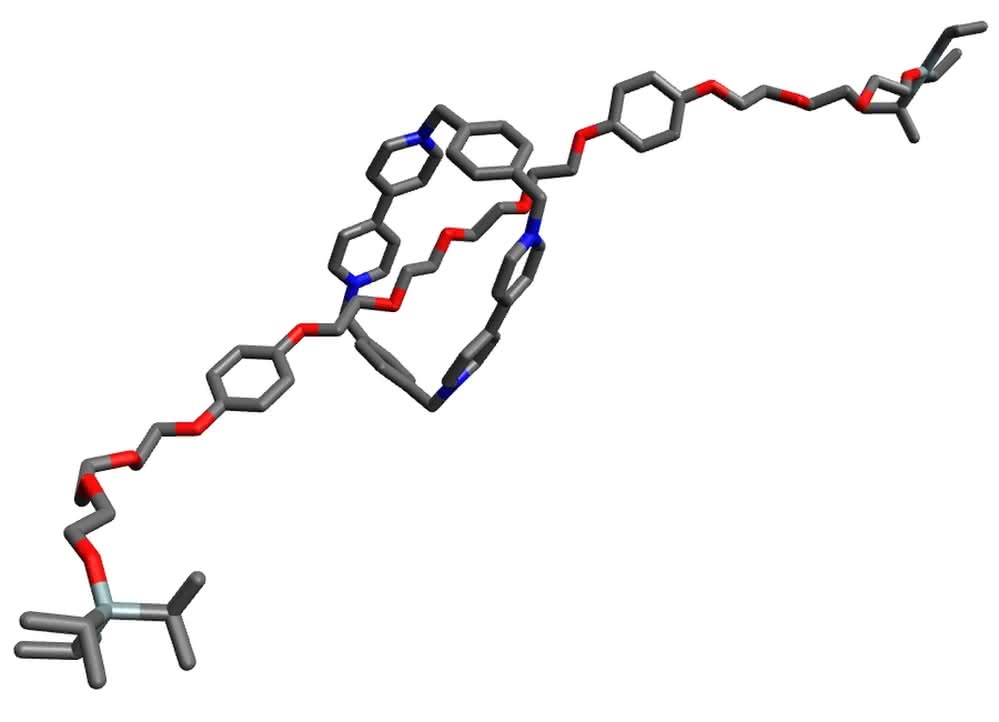
Molekuły połączone wiązaniem mechanicznym bardzo interesowały również wspomnianego już Frasera Stoddarta. W roku 1991 otrzymał on nowy rodzaj tych cząsteczek, zwany rotaksanami. W tym celu prowadził reakcję, w której dochodziło do połączenia końców długiej cząsteczki. Jednak Stoddard chciał, by przez utworzony w ten sposób pierścień przechodziła na podobieństwo osi inna cząsteczka o dużej długości. Aby pomóc w takim właśnie ułożeniu molekuł, na osi oraz w zamykającym się pierścieniu znajdowały się fragmenty, które wzajemnie się przyciągały. Spadaniu kółka z osi zapobiegały stopery, czyli duże fragmenty na jej końcach.
Kolejnym krokiem w stronę maszyn molekularnych było wprawienie w ruch pierścienia znajdującego się na osi. Przez odpowiednie zmiany potencjału elektrycznego przemieszczał się on od jednego do drugiego końca. Cały układ mógł więc działać jako np. przełącznik czy też przenośnik.
…winda, pamięć, siłownik…
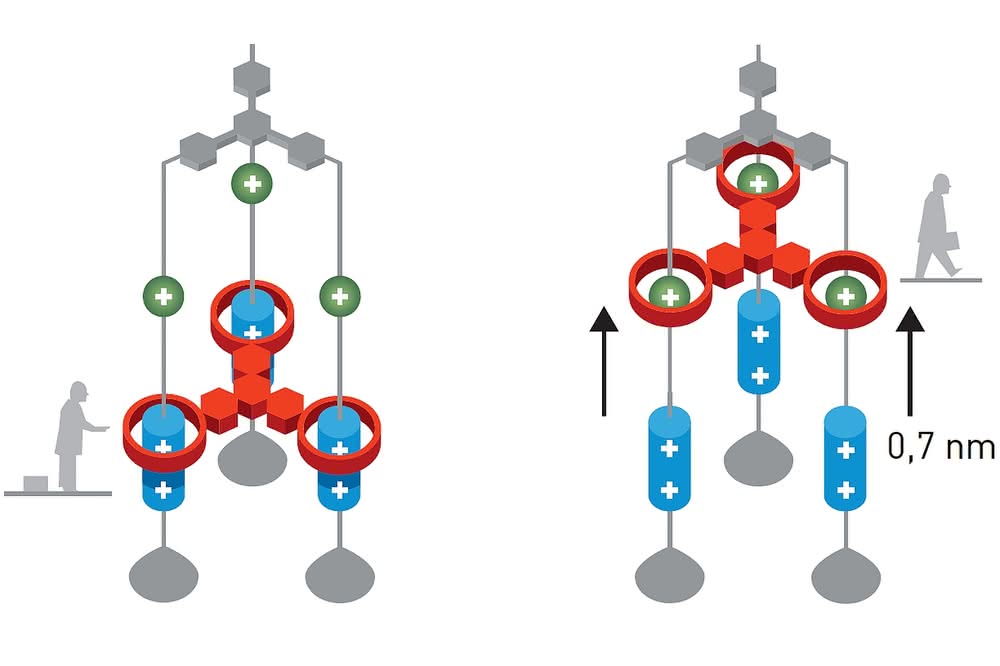
W latach 90. ubiegłego wieku zespół kierowany przez Stoddarta skonstruował molekularną windę. Była ona rotaksanem składającym się z trzech połączonych nici ze stoperami na końcach. Po osiach poruszał się układ trzech związanych ze sobą pierścieni (każdy pierścień po osobnej osi). Zmieniając potencjał elektryczny fragmentów osi, wymuszano ruch pierścieni tworzących platformę. Przemieszczenie odbywało się na dystansie 0,7 nm (1 nm = 10-9 m), co odpowiada kilkunastu średnicom atomowym. Siłę nośną windy oszacowano na dochodzącą do 200 pN (1 pN = 10-12 N). Masy atomów mieszczą się w granicach 10-25÷10-26 kg, zatem osiągi windy są całkiem dobre (dociekliwy czytelnik sam policzy, ile atomów może ona podnieść w ziemskim polu grawitacyjnym).
Innym osiągnięciem Stoddarta była konstrukcja układu elektronicznego, którego rdzeń stanowiły rotaksany (jako bramki logiczne i komórki pamięci). W roku 2007 osiągnięto pojemność 160 kilobitów i gęstość ok. 100 gigabitów/cm2 (kilkaset rotaksanów odpowiadało za przechowywanie stanu jednego bitu). Dla porównania: gęstość zapisu na zwykłej płycie CD to ok. 0,15 gigabitów/cm2.
Grupa Sauvage’a nie pozostawała w tyle i w roku 2000 splotła ze sobą dwie cząsteczki, które na jednym z końców miały pierścienie, a na drugim stopery uniemożliwiające rozłączenie konstrukcji. W powstałym rotaksanie oba fragmenty mogły się zbliżać, a następnie oddalać. Układ działał jak klasyczny siłownik lub ludzki mięsień, np. w jednym z eksperymentów zginał cienką złotą folię.
…i wreszcie silnik
Silniki to kluczowe elementy prawie każdej maszyny. W roku 1999 Ben Feringa dokonał syntezy pierwszej molekuły pełniącej jego rolę. Składała się ona z dwóch części, z których jedna mogła wirować tylko w określonym kierunku, a druga blokowała jej obroty wsteczne. Dzięki następującym po sobie pulsom promieniowania nadfioletowego oraz ogrzewaniu udało się wymusić kontrolowany ruch fragmentu cząsteczki. W roku 2014 silnik Feringi osiągnął aż 12 tys. obrotów na sekundę.
Silniki molekularne zastosowano do użytecznej pracy. W roku 2006 zakotwiczono napędy w podłożu, a na ich powierzchni położono szklany walec o rozmiarach rzędu tysięcznych części milimetra. Niewiele, ale to i tak ponad 10 tys. razy więcej, niż wynosi wielkość pojedynczego silnika. Po oświetleniu powierzchni cylinder ruszył naprzód, popychany ruchem wirników. Innym osiągnięciem grupy Feringi była konstrukcja samochodu, którego koła stanowiły obracające się rotory silników. Nanocar Feringi jeździł po oświetleniu promieniowaniem nadfioletowym o odpowiednio dobranej długości fali.
I co dalej?
Na przykład - molekularne roboty. Jeden z nich został skonstruowany w roku 2013 na bazie rotaksanów i umie przenosić oraz łączyć ze sobą aminokwasy (jak podczas syntezy białek w komórkach organizmach żywych). Zastosowań dla nanomaszyn na pewno nie zabraknie (medycyna, genetyka, informatyka itd.), a ograniczeniem może być tylko nasza wyobraźnia. Uzasadniając nagrodę, Komitet Noblowski zauważył, że maszyny molekularne znajdują się obecnie na takim samym etapie rozwoju, jak silniki elektryczne w latach 30. XIX wieku. Nikt chyba wtedy nie przypuszczał, patrząc na owe laboratoryjne zabawki, że w ciągu kilkudziesięciu lat staną się urządzeniami napędzającymi tramwaje, pociągi, samochody i wiele innych maszyn. Zważywszy, że tempo rozwoju nauki i techniki jest obecnie nieporównywalnie większe niż dwieście lat temu, z pewnością wkrótce ujrzymy praktyczne zastosowanie konstrukcji Sauvage’a, Stoddarta i Feringi.
 Jean-Pierre Sauvage (ur. w 1944 r. w Paryżu) jest emerytowanym profesorem chemii Uniwersytetu w Strasburgu. Zajmował się chemią koordynacyjną oraz katenanami i maszynami molekularnymi.
Jean-Pierre Sauvage (ur. w 1944 r. w Paryżu) jest emerytowanym profesorem chemii Uniwersytetu w Strasburgu. Zajmował się chemią koordynacyjną oraz katenanami i maszynami molekularnymi. Sir James Fraser Stoddart (ur. w 1942 r. w Edynburgu) jest szkockim chemikiem zatrudnionym na Northwestern University (Evaston w stanie Illinois, USA). Pracuje nad syntezą katenanów i rotaksanów oraz ich wykorzystaniem do konstrukcji maszyn molekularnych. Wychował się na farmie, w której nie było telewizji ani elektryczności. Uważa, że układanie w dzieciństwie puzzli oraz innych łamigłówek pozwoliło mu wytrenować wyobraźnię przestrzenną.
Bernard Lucas „Ben” Feringa (ur. w 1951 r. w Barger-Compascuum w Holandii) jest związany z Uniwersytetem w Groningen. Zajmuje się katalizą oraz molekularnymi przełącznikami i silnikami. Twierdzi, że siła chemii polega nie tyle na poznaniu właściwości już istniejących związków, ile na tworzeniu materiałów, których nie ma w naturze.