Pierwiastkowa arystokracja

Z biegiem czasu "poszły do pracy", a w drugiej połowie ubiegłego wieku zaczęły wiązać się z mniej szlachetnymi pierwiastkami. Opowieść o pierwiastkowych wyższych sferach zacznijmy tak:
Dawno, dawno temu…
…był pewien lord.
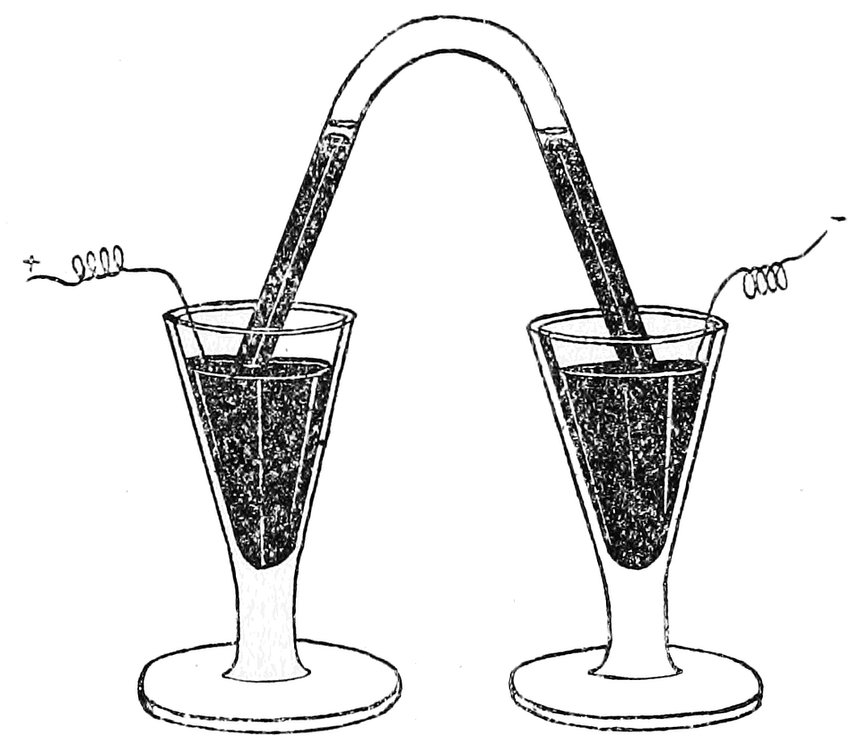
Henry Cavendish należał do najwyższej brytyjskiej arystokracji, ale interesowało go badanie tajników przyrody. W roku 1766 odkrył wodór, a dziewiętnaście lat później przeprowadził eksperyment, w którym mógł znaleźć kolejny pierwiastek. Chciał się przekonać, czy powietrze oprócz znanych już tlenu i azotu, zawiera również inne składniki. Zgiętą szklaną rurę wypełnił powietrzem, jej końce zanurzył w naczyniach z rtęcią i przepuszczał pomiędzy nimi wyładowania elektryczne. Iskry sprawiały, że azot łączył się z tlenem, a wytworzone kwaśne związki były pochłaniane przez roztwór zasady. Gdy brakło tlenu, Cavendish wprowadzał go do rury i kontynuował doświadczenie, aż do usunięcia całego azotu. Eksperyment trwał kilka tygodni, podczas których ciągle zmniejszała się objętość gazu w rurze. Gdy już wyczerpał się azot, Cavendish usunął tlen i stwierdził, że pozostał pęcherzyk, który ocenił na 1/120 początkowej objętości powietrza. Lord nie dociekał natury pozostałości, uznając efekt za błąd doświadczenia. Dziś wiemy, że był bardzo blisko odkrycia argonu, ale na dokończenie eksperymentu przyszło poczekać ponad wiek.
Słoneczna tajemnica
Zaćmienia Słońca zawsze stanowią wielką atrakcję, zarówno dla laików, jak i naukowców. 18 sierpnia 1868 r. astronomowie obserwujący to zjawisko po raz pierwszy użyli spektroskopu (skonstruowanego niespełna dekadę wcześniej) do zbadania protuberancji słonecznych, dobrze widocznych przy zasłoniętej tarczy. Francuz Pierre Janssen dowiódł w ten sposób, że korona słoneczna składa się głównie z wodoru oraz innych ziemskich pierwiastków. Ale następnego dnia, gdy ponownie obserwował Słońce, zauważył nieopisaną wcześniej linię widmową, położoną w pobliżu charakterystycznej żółtej linii sodu. Janssen nie był w stanie przypisać jej żadnemu ówcześnie znanemu pierwiastkowi. Taką samą obserwację wykonał również angielski astronom Norman Lockyer. Uczeni wysnuwali różne hipotezy dotyczące tajemniczego składnika naszej gwiazdy. Lockyer nadał mu nazwę hel, od imienia greckiego boga Słońca – Heliosa. Jednak większość naukowców uważała, że zauważona żółta linia to fragment widma wodoru znajdującego się w ekstremalnie wysokiej temperaturze panującej w gwieździe. W roku 1881 włoski fizyk i meteorolog Luigi Palmieri badał spektroskopem gazy wulkaniczne wydobywające się z Wezuwiusza. W ich widmie stwierdził obecność żółtego prążka przypisywanego helowi. Palmieri jednak niejasno opisał wyniki swoich doświadczeń, a inni naukowcy ich nie potwierdzili. Obecnie wiemy, że hel znajduje się w gazach wulkanicznych i Włoch rzeczywiście mógł być pierwszym, który obserwował widmo ziemskiego helu.
Odkrycie na trzecim miejscu po przecinku
W początkach ostatniej dekady XIX wieku brytyjski fizyk lord Rayleigh (John William Strutt) postanowił dokładnie oznaczyć gęstości różnych gazów, co pozwoliło również dokładnie określić masy atomowe wchodzących w ich skład pierwiastków. Rayleigh był starannym eksperymentatorem, więc otrzymywał gazy z różnych źródeł, aby wykryć domieszki fałszujące wyniki. Udało mu się zmniejszyć błąd oznaczenia do kilku setnych procenta, w owym czasie wielkości bardzo małej. Analizowane gazy wykazywały zgodność wyznaczonej gęstości w granicach błędu pomiaru. Nie zdziwiło to nikogo, wszak skład związków chemicznych jest niezależny od ich pochodzenia. Wyjątkiem był azot – jedynie on miał różną gęstość w zależności od sposobu uzyskania. Azot atmosferyczny (otrzymany z powietrza po oddzieleniu tlenu, pary wodnej i dwutlenku węgla) był zawsze cięższy niż chemiczny (pochodzący z rozkładu jego związków). Różnica – co zadziwiające – była stała i wynosiła ok. 0,1%. Rayleigh, który nie umiał wyjaśnić tego fenomenu, zwrócił się do innych uczonych.
Pomoc zaproponował chemik William Ramsay. Obaj naukowcy doszli do wniosku, że jedynym wytłumaczeniem jest obecność domieszki cięższego gazu w azocie otrzymanym z powietrza. Gdy natknęli się na opis eksperymentu Cavendisha, poczuli, że są na dobrym tropie. Powtórzyli doświadczenie, tym razem stosując już nowoczesną aparaturę, i wkrótce mieli do dyspozycji próbkę nieznanego gazu. Analiza przy pomocy spektroskopu wykazała jego odrębność od znanych substancji, a inne badania pozwoliły stwierdzić, że występuje on w postaci pojedynczych atomów. Do tej pory nie znano takich gazów (mamy O2, N2, H2), zatem równocześnie oznaczało to odkrycie nowego pierwiastka. Rayleigh i Ramsay usiłowali zmusić argon (gr. argos = leniwy) do reakcji z innymi substancjami, ale bez skutku. W celu określenia jego temperatury skraplania zwrócili się do jedynego wówczas na świecie człowieka, który dysponował odpowiednią aparaturą. Był to Karol Olszewski, profesor chemii Uniwersytetu Jagiellońskiego. Olszewski skroplił i zestalił argon, a także wyznaczył inne jego parametry fizyczne.
Doniesienie Rayleigha i Ramsaya z sierpnia 1894 r. wywołało olbrzymie poruszenie. Uczeni nie mogli uwierzyć, że całe pokolenia badaczy pominęły składnik powietrza stanowiący w nim prawie 1%, obecny na Ziemi w ilości znacznie większej niż np. srebro. Próby wykonane przez innych potwierdziły istnienie argonu. Odkrycie słusznie uważano za wielkie osiągnięcie i triumf starannego eksperymentu (mawiano, że nowy pierwiastek krył się na trzecim miejscu po przecinku). Nikt jednak nie przypuszczał, że w powietrzu znajduje się…
…cała rodzina gazów.
Zanim jeszcze dokładnie przeanalizowano skład atmosfery, rok później Ramsaya zaciekawiła notatka w czasopiśmie geologicznym, w której donoszono o gazie wydzielającym się z rud uranu pod wpływem kwasu. Ramsay powtórzył próbę, zbadał otrzymany gaz spektroskopem i dostrzegł nieznane mu linie widmowe. Konsultacja z Williamem Crookesem, specjalistą od spektroskopii, pozwoliła stwierdzić, że jest to od dawna poszukiwany na Ziemi hel. Obecnie już wiemy, że stanowi on jeden z produktów rozpadu uranu i toru, który został uwięziony w rudach naturalnych pierwiastków promieniotwórczych. Ramsay ponownie zwrócił się do Olszewskiego o skroplenie nowego gazu. Tym razem jednak możliwości aparatury nie pozwoliły osiągnąć dostatecznie niskich temperatur i ciekły hel otrzymano dopiero w roku 1908.
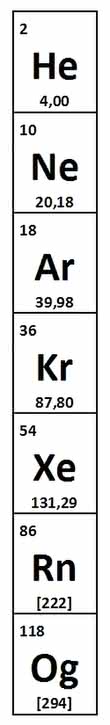
Hel również okazał się gazem jednoatomowym i nieczynnym jak argon. Właściwości obu pierwiastków nie pasowały do żadnej rodziny układu okresowego i postanowiono utworzyć dla nich oddzielną grupę. [helowce_uklad] Ramsay doszedł do wniosku, że są w niej luki i wraz ze swym współpracownikiem Morrisem Traversem rozpoczęli dalsze badania. W wyniku destylacji ciekłego powietrza chemicy odkryli w roku 1898 trzy następne gazy: neon (gr. neos = nowy), krypton (gr. kryptos = skryty) i ksenon (gr. ksenos = obcy). Wszystkie one wraz z helem występują w powietrzu w minimalnych ilościach, znacznie mniejszych niż argon. Chemiczna bierność nowych pierwiastków zasugerowała badaczom nadanie im wspólnego miana gazów szlachetnych.
Po nieudanych próbach wydzielenia z powietrza, kolejny helowiec odkryto jako produkt przemian promieniotwórczych. W roku 1900 Friedrich Dorn oraz André-Louis Debierne zauważyli wydzielanie gazu (emanacji, jak wtedy mówiono) z radu, któremu nadali nazwę radon. Niedługo potem zaobserwowano, że emanacje wydzielają również tor i aktyn (toron i aktynon). Ramsay i Frederick Soddy dowiedli, że stanowią one jeden pierwiastek i są kolejnym gazem szlachetnym, który nazwali nitonem (łac. niteo = błyszczeć, ponieważ próbki gazu świeciły w ciemnościach). W roku 1923 niton stał się ostatecznie radonem, od nazwy najdłużej żyjącego izotopu.
Ostatni z helowców, zamykający obecny układ okresowy, otrzymano w roku 2006 w rosyjskim laboratorium jądrowym w Dubnej. Nazwa, zatwierdzona dopiero dziesięć lat później, to oganesson, na cześć rosyjskiego fizyka jądrowego Jurija Oganiesjana. O nowym pierwiastku wiadomo tylko tyle, że jest najcięższym z dotychczas znanych i że otrzymano zaledwie kilka jego jąder, które żyły niespełna milisekundę.
Chemiczne mezalianse
Przekonanie o chemicznej bierności helowców runęło w roku 1962, gdy Neil Bartlett otrzymał związek o wzorze Xe[PtF6]. Chemia związków ksenonu jest dziś dość obszerna: znane są fluorki, tlenki, a nawet sole kwasów tego pierwiastka. W dodatku są to połączenia trwałe w normalnych warunkach. Lżejszy od ksenonu krypton tworzy kilka fluorków, podobnie jak cięższy radon (promieniotwórczość tego ostatniego znacznie utrudnia badania). Natomiast trzy najlżejsze – hel, neon i argon – nie mają żadnych trwałych połączeń.
Związki chemiczne gazów szlachetnych z mniej szlachetnymi partnerami można porównać do dawnych mezaliansów. Dziś już to pojęcie nie ma racji bytu, nie powinien też budzić zdziwienia fakt, że i…
…arystokraci pracują.
Helowce otrzymuje się przez rozdział skroplonego powietrza w wytwórniach azotu i tlenu. Źródłem helu jest natomiast głównie gaz ziemny, w którym stanowi on nawet do kilku procent objętości (w Europie największa instalacja produkująca hel pracuje w Odolanowie, w województwie wielkopolskim). Pierwszym ich zajęciem było świecenie w rurkach jarzeniowych. Obecnie nadal cieszą oczy neonowe reklamy, ale helowce są także sercem niektórych typów laserów, np. lasera argonowego, który spotkamy u dentysty czy kosmetyczki.
Chemiczną bierność helowców wykorzystuje się do wytwarzania atmosfery chroniącej przed utlenieniem, np. podczas spawania metali czy w hermetycznych opakowaniach żywności. Żarówki napełnione helowcami pracują w wyższej temperaturze (czyli jaśniej świecą) i oszczędniej zużywają energię elektryczną. Zwykle stosuje się argon w mieszaninie z azotem, a jeszcze lepsze rezultaty zapewniają krypton i ksenon. Najnowsze zastosowanie ksenonu to materiał napędowy w rakietowym silniku jonowym, bardziej wydajnym niż silniki na paliwa chemiczne. Najlżejszym helem napełnia się balony meteorologiczne i baloniki dla dzieci. W mieszaninie z tlenem hel używany jest przez nurków do prac na dużych głębokościach, co pozwala im uniknąć choroby kesonowej. Najważniejszym zastosowaniem helu jest uzyskiwanie niskich temperatur, niezbędnych do działania nadprzewodników.