Benzen w 126 wymiarach
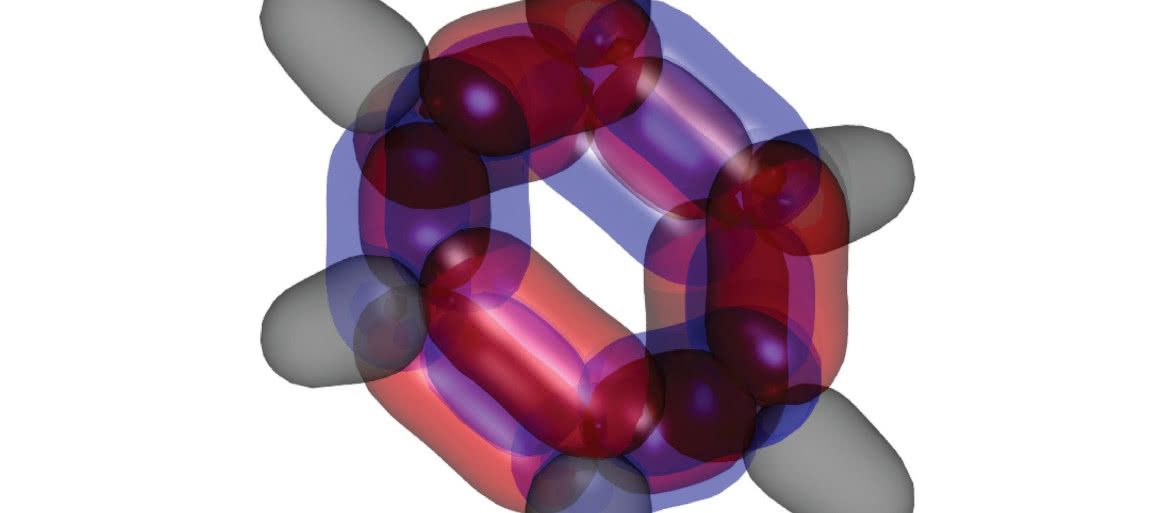
Benzen to organiczny związek chemiczny z grupy arenów. Jest to najprostszy karbocykliczny, obojętny węglowodór aromatyczny. Jest on m.in. składnikiem DNA, białek, drewna i ropy naftowej. Problem budowy benzenu interesował chemików już od chwili wyodrębnienia tego związku. W 1865 r. niemiecki chemik Friedrich August Kekulé wysunął hipotezę, że benzen jest cykloheksatrienem o sześcioczłonowym pierścieniu, w którym pomiędzy atomami węgla na przemian występują wiązania pojedyncze i podwójne.
Od lat 30. XX wieku w kręgach chemicznych toczy się debata na temat budowy cząsteczki benzenu. Jest to debata, która w ostatnich latach nabrała dodatkowej ostrości, ponieważ benzen, który składa się z sześciu atomów węgla połączonych z sześcioma atomami wodoru, jest najmniejszą znaną cząsteczką, jaką można wykorzystać w produkcji materiałów optoelektronicznych, przyszłościowej dziedziny techniki.
Kontrowersje wokół struktury cząsteczki pojawiają się, ponieważ choć ma ona niewiele komponentów atomowych, istnieje w stanie matematycznie opisywanym nie przez trzy, a nawet cztery wymiary (z włączeniem czasu), jakie znamy z naszych doświadczeń, ale przez aż 126 wymiarów.
Skąd ta liczba? Stąd, że każdy z 42 elektronów wchodzących w skład cząsteczki jest opisywany w trzech wymiarach a pomnożenie ich przez liczbę cząstek daje właśnie 126. Nie są to zatem rzeczywiste, lecz matematyczne wymiary. Pomiar tego złożonego, i bardzo małego układu jak do tej pory okazywał się niemożliwy, co oznaczało, że dokładne zachowanie elektronów w benzenie nie mogło zostać poznane. A to stanowiło problem, ponieważ bez tej informacji nigdy nie będzie można w pełni opisać trwałości molekuły w zastosowaniach technicznych.
Teraz jednak naukowcom kierowanym przez Timothy’ego Schmidta z ARC Centre of Excellence in Exciton Science i Uniwersytetu Nowej Południowej Walii w Sydney udało się rozwikłać tę tajemnicę. Wraz z kolegami z UNSW i ośrodka CSIRO Data61, zastosował złożoną metodę opartą na algorytmach, zwaną próbkowaniem dynamicznym Voronoi Metropolis (DVMS) do cząsteczek benzenu w celu mapowania ich falowych funkcji we wszystkich 126 wymiarach. Algorytm ten pozwala na podział przestrzeni wymiarowej na "kafelki", z których każdy odpowiada permutacjom pozycji elektronów. Wyniki tych badań zostały opublikowane w czasopiśmie "Nature Communications".
Szczególnie interesujące dla naukowców było zrozumienie spinu elektronów. "To, co odkryliśmy, było bardzo zaskakujące", zauważa w publikacji profesor Schmidt. "Elektrony w podwójnym wiązaniu węglowym o spinie skierowanym ku górze łączyły się w trójwymiarowe konfiguracje o mniejszej energii. Zasadniczo zmniejsza to energię cząsteczki, czyniąc ją bardziej stabilną, dzięki odpychającym się i schodzącym sobie z drogi elektronom". Stabilność cząsteczki to z kolei cecha pożądana w zastosowaniach technicznych.
Mirosław Usidus