Kopiuj i wklej - do projektowania ludzi jeden krok
Huxley pisał o "wybutlowywaniu" dzieci o pożądanych cechach wyglądu i charakteru, uwzględniając kwestie zarówno samych urodzin, jak i późniejszego warunkowania do życia w wyidealizowanym społeczeństwie.
"Ulepszanie ludzi będzie najprawdopodobniej największym przemysłem XXI wieku", prognozuje Yuval Harari, autor niedawno wydanej książki "Homo Deus". Jak zauważa izraelski historyk, nasze ciała wciąż pracują na tym samym hardwarze i softwarze co 200 tys. lat temu. Dodaje jednak, że solidny upgrade człowieka może być dość drogi, co spowoduje, że nierówności społeczne zyskają zupełnie nowy wymiar. "Po raz pierwszy w historii nierówność ekonomiczna może oznaczać także nierówność biologiczną", pisze Harari.
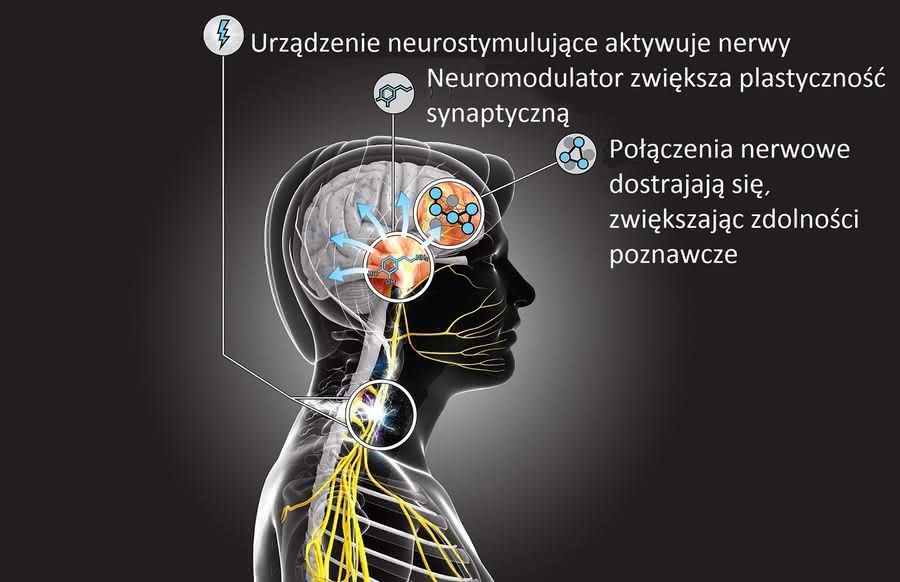
Starym marzeniem fantastów jest opracowanie techniki szybkiego i bezpośredniego "załadunku" wiedzy i umiejętności do mózgu. Okazuje się, że agencja DARPA zainaugurowała projekt badawczy, którego celem jest właśnie coś takiego. Program o nazwie Targeted Neuroplasticity Training (TNT) ma na celu przyspieszenie procesu nabywania nowej wiedzy przez umysł człowieka, za pomocą manipulacji wykorzystujących plastyczność synaptyczną. Badacze wierzą, że przez neurostymulację synaps można je przestawić na bardziej regularny i uporządkowany mechanizm tworzenia połączeń, które są istotą nauki.
CRISPR jak MS Word
Choć w tej chwili wydaje się nam to mało wiarygodne, ze świata nauki wciąż dobiegają zapowiedzi, że kres śmiertelnych chorób jest bliski. Choćby nowotworów. Immunoterapia polegająca na wyposażaniu pobranych od pacjenta komórek układu immunologicznego w molekuły "odpowiadające" rakowi, przynosi zdumiewające sukcesy. Podczas badań u 94% (!) pacjentów z ostrą białaczką limfoblastyczną znikły objawy choroby. U pacjentów z chorobami nowotworowymi krwi odsetek ten wynosi 80%.
A to dopiero wstęp, bo prawdziwym hitem ostatnich miesięcy jest technika edycji genów CRISPR. Dopiero ona czyni proces edycji genów czymś, co niektórzy porównują do edycji tekstu w MS Wordzie - działaniem wydajnym i stosunkowo prostym.
CRISPR to skrót od angielskiego terminu clustered regularly interspaced short palindromic repeats ("zgromadzone regularnie przerywane krótkie powtórzenia palindromiczne"). Metoda polega na edytowaniu kodu DNA (wycinaniu popsutych fragmentów, zastępowaniu ich nowymi lub dopisywaniu fragmentów kodu DNA, zupełnie jak w przypadku edytorów tekstu) - tak, by naprawić komórki zaatakowane przez raka, a nawet by całkiem raka zniszczyć, wyeliminować z komórek. CRISPR ponoć naśladuje naturę, a konkretnie metodę, jaką stosowały bakterie do obrony w przypadku ataku przez wirusy. Inaczej niż w przypadku GMO, zmiana w genach nie wiąże się jednak z wprowadzaniem genów innych gatunków.
Historia metody CRISPR zaczyna się w 1987 r. Zespół japońskich badaczy znalazł wtedy niezbyt typowe fragmenty DNA w genomie bakterii Escherichia coli. Miały one postać pięciu identycznych sekwencji, porozdzielanych całkowicie odmiennymi odcinkami. Naukowcy nie rozumieli tego. Sprawa wzbudziła większe zainteresowanie dopiero wówczas, gdy podobne sekwencje DNA wykryto także u innych gatunków bakterii. Musiały więc w komórkach służyć do czegoś ważnego. W 2002 r. Ruud Jansen z holenderskiego Uniwersytetu w Utrechcie postanowił nadać tym sekwencjom nazwę CRISPR. Zespół Jansena odkrył też, że tajemniczym sekwencjom zawsze towarzyszył gen kodujący enzym, o nazwie Cas9, który potrafi ciąć nić DNA.
Po kilku latach uczeni pojęli, jaka jest funkcja tych sekwencji. Gdy wirus atakuje bakterię, enzym Cas9 chwyta jego DNA, tnie i wciska między identyczne sekwencje CRISPR w bakteryjnym genomie. Wzór ten przydaje się wtedy, gdy bakteria znów zostanie zaatakowana przez wirus tego samego typu. Wówczas bakteria od razu go rozpozna i zniszczy. Naukowcy po kolejnych latach badań doszli do wniosku, że CRISPR w połączeniu z enzymem Cas9 można wykorzystać do manipulowania DNA w laboratorium. Zespoły badawcze Jennifer Doudna z Uniwersytetu Berkeley w USA i Emmanuelle Charpentier z Uniwersytetu Umea w Szwecji ogłosiły w 2012 r., że bakteryjny system po zmodyfikowaniu pozwala na edycję dowolnego fragmentu DNA: można z niego wycinać geny, wstawiać nowe, włączać je lub wyłączać.
Sama metoda, nazwana CRISPR-Cas9, działa na zasadzie rozpoznawania obcego DNA dzięki mRNA, które odpowiada za przenoszenie informacji genetycznej. Cała sekwencja CRISPR dzielona jest następnie na krótsze kawałki (crRNA) zawierające fragment DNA wirusa oraz sekwencję CRISPR. Na podstawie tej informacji zawartej w sekwencji CRISPR tworzony jest tracrRNA, który doczepia się do crRNA, tworzone razem przez gRNA, będący swoistym zapisem wirusa, jego sygnaturą -zapamiętywanym przez komórkę i wykorzystywanym w walce z wirusem.
W przypadku infekcji, gRNA, które jest wzorcem atakującego wirusa, łączy się z enzymem Cas9 i tnie napastnika na kawałki, całkowicie go unieszkodliwiając. Wycięte kawałki są potem dodawane do sekwencji CRISPR, swoistej bazy danych o zagrożeniach. Podczas dalszego opracowywania techniki okazało się, że gRNA może być tworzony przez człowieka, dzięki czemu da się ingerować w geny, podstawiać w nich lub wycinać niebezpieczne fragmenty.
W ubiegłym roku onkolodzy z Uniwersytetu Syczuańskiego w Chengdu rozpoczęli test techniki edytowania genów metodą CRISPR-Cas9. To był pierwszy raz, gdy tę rewolucyjną metodę testowano na człowieku chorym na nowotwór. Pacjent cierpiący na agresywnego raka płuc otrzymał komórki zawierające zmodyfikowane geny, które mają pomóc mu w zwalczeniu choroby. Pobrano od niego komórki, wycięto z nich gen, który miałby osłabiać działanie jego własnych komórek przeciw komórkom rakowym i wprowadzono je z powrotem do pacjenta. Takie zmodyfikowane komórki powinny lepiej poradzić sobie z rakiem.
Ta technika, oprócz niskiego kosztu i prostoty, ma też inną ogromną zaletę - zanim wprowadzi się ponownie zmodyfikowane komórki, można je starannie przetestować, bo modyfikuje się je poza pacjentem. Pobiera się jego krew, przeprowadza się odpowiednie manipulacje, wybiera się odpowiednie komórki i dopiero wówczas się je podaje. Bezpieczeństwo jest znacznie większe, niż gdybyśmy podawali takie komórki bezpośrednio i czekali na to, co się wydarzy.
Designer baby, czyli zaprogramowane genetycznie dziecko
Co możemy zmienić za pomocą inżynierii genetycznej? Okazuje się, że bardzo dużo. Pojawiają się doniesienia o zastosowaniu tej metody do zmiany DNA roślin, pszczół, świń, psów, a nawet ludzkich zarodków. Mamy informacje o roślinach uprawnych, które potrafią bronić się przed atakującymi je grzybami, o warzywach o przedłużonej świeżości lub zwierzętach hodowlanych uodpornionych na groźne wirusy. CRISPR pozwolił także na prace nad modyfikowaniem komarów, które roznoszą malarię. Za pomocą CRISPR udało się wprowadzić do DNA tych owadów gen odporności na mikroby. I to w taki sposób, że dziedziczy go całe ich potomstwo - bez wyjątków.
Łatwość zmiany kodów DNA rodzi jednak wiele dylematów natury etycznej. O ile używanie tej metody do leczenia chorych na raka nie wzbudza wątpliwości, to nieco inaczej dzieje się, gdy zaczynamy rozważać jej stosowanie do leczenia skłonności do otyłości czy nawet do kwestii posiadania blond włosów. Gdzie postawić granicę ingerencji w ludzkie geny? Zmiana genu chorego może być akceptowalna, ale już zmiana genów u embrionów przeniesie się również automatycznie na kolejne pokolenia, co może być wykorzystywane dla dobra, ale też i wbrew dobru, ludzkości.
W 2014 r. pewien amerykański badacz ogłosił, że zmodyfikował wirusy tak, by wprowadzały elementy CRISPR do myszy. Tam spreparowany DNA uaktywniał się, powodując mutację, która wywoływała odpowiednik ludzkiego raka płuc… W podobny sposób można by teoretycznie stworzyć broń biologiczną, wywołującą nowotwory u ludzi. W 2015 r. chińscy uczeni poinformowali, że wykorzystali CRISPR do modyfikacji w ludzkich zarodkach genów, których mutacje prowadzą do dziedzicznej choroby zwanej talasemią. Zabieg wywołał kontrowersje. Dwa najważniejsze czasopisma naukowe świata - "Nature" i "Science" - odmówiły opublikowania pracy Chińczyków. Ukazała się ona w końcu w piśmie "Protein & Cell". Przy okazji pojawiły się informacje, że co najmniej cztery inne zespoły badawcze w Chinach też pracują nad modyfikacjami genetycznymi ludzkich zarodków. Pierwsze wyniki tych prac już znamy - uczeni wstawili do DNA zarodka gen dający odporność na zakażenie wirusem HIV.
Wielu ekspertów wyraża pewność, że narodziny dziecka ze zmodyfikowanymi sztucznie genami są już tylko kwestią czasu.